| קתפסין | |||||||||
|---|---|---|---|---|---|---|---|---|---|
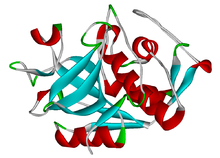 מבנה קתפסין K | |||||||||
| מזהים | |||||||||
| סֵמֶל | CTP | ||||||||
| פפאם | PF00112 | ||||||||
| פפאם שֶׁבֶט | CL0125 | ||||||||
| אינטרפרו | IPR000668 | ||||||||
| לִכאוֹב | Pept_C1 | ||||||||
| PROSITE | PDOC00126 | ||||||||
| MEROPS | C1 | ||||||||
| SCOP2 | 1aec / תְחוּם / SUPFAM | ||||||||
| |||||||||
Cathepsins (יוון העתיקה קטה- "למטה" ו hepsein "רְתִיחָה"; מְקוּצָר CTS) הם פרוטאזות (אנזימים המשפילים חלבונים) הנמצאים בכל בעלי החיים וכן באורגניזמים אחרים. ישנם כתריסר בני משפחה זו, אשר נבדלים על ידי המבנה שלהם, מנגנון קטליטי, ואילו חלבונים הם מפלחים[צורך בציטוט ]. מרבית החברים הופעלים ב pH נמוך הנמצא ב ליזוזומים. לפיכך, הפעילות של משפחה זו נעוצה כמעט לחלוטין בתוך אלה אברונים. ישנם, עם זאת, יוצאים מן הכלל כגון קתפסין ק, שעובד חוץ תאית לאחר הפרשתו על ידי אוסטאוקלסטים ב ספיגת עצם. לקתפסינים יש תפקיד חיוני במחזור הסלולר של יונקים.
מִיוּן
- קתפסין א (פרוטאז סריני )
- קתפסין ב (פרוטאז ציסטאין )
- קתפסין ג (פרוסטאז ציסטאין)
- קתפסין ד (פרוטאז אספרטיל )
- קתפסין E (פרוטאז אספרטיל)
- קתפסין F (חלבון ציסטאין)
- קתפסין ג'י (פרוטאז סרין)
- קתפסין ח (פרוסטאז ציסטאין)
- קתפסין ק (פרוסטאז ציסטאין)
- קתפסין L1 (פרוסטאז ציסטאין)
- קתפסין L2 (או V) (פרוסטאז ציסטאין)
- קתפסין או (פרוסטאז ציסטאין)
- קתפסין ס (פרוסטאז ציסטאין)
- קתפסין W. (חלבון ציסטאין)
- קתפסין זי (או X) (פרוסטאז ציסטאין)
משמעות קלינית
Cathepsins היו מעורבים ב:
- מחלת הסרטן, קתפסין D הוא א מיטוגן ו"זה מחליש את התגובה החיסונית נגד הגידול של כימוקינים מתפוררים כדי לעכב את תפקודם של תאי הדנדריטים ". Cathepsins B ו- L מעורבים בפירוק מטריקס ובפלישת תאים.[1]
- שבץ[2]
- פגיעה מוחית טראומטית[3]
- מחלת אלצהיימר[4]
- דַלֶקֶת פּרָקִים[5]
- אבולה, נמצא כי קתפסין B ובמידה פחותה קתפסין L נחוצים לצורך כניסת הנגיף לתאי המארח.[6]
- COPD
- דלקת חניכיים כרונית
- דלקת הלבלב
- מספר הפרעות בעין: קרטוקונוס, ניתוק רשתית, ניוון מקולרי הקשור לגיל, ו בַּרקִית.[7]
קתפסין א
ליקויים בחלבון זה קשורים למספר צורות של גלקטוזיאלידוזיס. פעילות הקתפסין A ב lysates של נגעים גרורתיים של מלנומה ממאירה הוא גבוה משמעותית מאשר ב lysates המוקד העיקרי. קתפסין A גדל בשרירים המושפעים בינוני ממחלת ניוון שרירים ומחלות מפרקים.
קתפסין ב
קתפסין ב עשוי לתפקד כ- בטא-סיקרטאז 1, ביקוע חלבון מבשר עמילואיד כדי לייצר בטא עמילואיד.[8] ביטוי יתר של החלבון המקודד, שהוא בן למשפחת הפפטידאז C1, נקשר אדנוקרצינומה של הוושט וגידולים אחרים.[9] קתפסין B היה מעורב גם בהתקדמות של גידולים אנושיים שונים[1] לְרַבּוֹת סרטן שחלות.
קתפסין ד
קתפסין D (an פרוטאז אספרטיל ) נראה כי הוא מבקע מגוון של מצעים כגון פיברונקטין ו למינין. בניגוד לחלק מהקתפסינים האחרים, לקתפסין D יש פעילות פרוטאזית מסוימת ב- pH ניטראלי.[10] נראה כי רמות גבוהות של אנזים זה בתאי הגידול קשורות לפולשנות רבה יותר.
קתפסין ק
קתפסין K הוא היונק הכי חזק קולגן. קתפסין K מעורב ב אוסטאופורוזיס, מחלה שבה ירידה בצפיפות העצם גורמת לסיכון מוגבר לשברים. אוסטאוקלסטים הם תאי הגוף המחזירים עצם, והם מפרישים קתפסין K על מנת להתפרק קולגן, המרכיב העיקרי של מטריצת החלבון הלא-מינרלית של העצם.[11] קתפסין K, בין שאר הקתפסינים, ממלא תפקיד בגרורות סרטן באמצעות השפלה של המטריצה החוץ תאית.[12] נוקאאוט הגנטי של קתפסין S ו- K בעכברים עם טרשת עורקים הוכח כמפחית את גודל הנגעים הטרשיים.[13] הביטוי של קתפסין K בתאי אנדותל מתורבת מווסת על ידי מתח גזירה.[14] הוכח כי קתפסין K ממלא תפקיד בדלקת פרקים.[15]
קתפסין V.
קתפסין L עכבר הוא הומולוגי לקתפסין אנושי V.[16] הוכח כי קתפסין עכבר L ממלא תפקיד באדיפוגנזה ובאי סבילות לגלוקוז בעכברים. קתפסין L משפיל את פיברונקטין, קולטן לאינסולין (IR), ו- קולטן גורם 1 לגידול באינסולין (IGF-1R). הוכח שיש לעכברים עם חסר ל- Cathepsin L שיש פחות רקמת שומן, רמות גלוקוז ואינסולין בסרום נמוכות יותר, יותר יחידות תת קולטן לאינסולין, יותר טרנספורטר גלוקוז (GLUT4) ויותר פיברונקטין מאשר בקרות מסוג בר.[17]
מעכבים
חמישה פפטידים מחזוריים מראים פעילות מעכבת כלפי קתפסינים אנושיים L, B, H ו- K.[18]
זימוגרפיה של קתפסין
זמוגרפיה הוא סוג של אלקטרופורזה ג'ל המשתמשת ב- פוליאקרילאמיד לְהַגלִיד שיתוף פולימר עם מצע על מנת לזהות פעילות אנזימים. זימוגרפיה של קתפסין מפרידה בין קתפסינים שונים על בסיס נדידתם באמצעות ג'ל פוליאקרילאמיד המפולימר יחד ג'לטין מצע. האלקטרופורזה מתרחשת בתנאים שאינם מצמצמים, והאנזימים מוגנים מפני דנטורציה באמצעות ליופפטין.[19] לאחר קביעת ריכוז החלבון נטענים כמויות שוות של חלבון רקמות בג'ל. לאחר מכן מותר לחלבון לנדוד דרך הג'ל. לאחר אלקטרופורזה, מכניסים את הג'ל למאגר מחדש על מנת להחזיר את הקתפסינים לקונפורמציה המקורית שלהם. לאחר מכן מכניסים את הג'ל למאגר הפעלה של pH ספציפי ומניחים לדגור בן לילה ב 37 מעלות צלזיוס. שלב הפעלה זה מאפשר לקתפסינים לבזות את מצע הג'לטין. כאשר הג'ל מוכתם באמצעות כתם כחול של קומאסי, אזורי הג'ל שעדיין מכילים ג'לטין נראים כחולים. אזורי הג'ל בהם פעלו קתפסינים נראים כפסים לבנים. זֶה צימפסוגרפיה של קתפסין פרוטוקול שימש לאיתור כמויות פמטומול של קתפסין בוגר.[19] ניתן לזהות את הקתפסינים השונים בהתבסס על מרחק הנדידה שלהם בשל משקלם המולקולרי: קתפסין K (~ 37 kDa), V (~ 35 kDa), S (~ 25kDa) ו- L (~ 20 kDa). לקתפסינים יש רמות pH ספציפיות בהן יש להם פעילות פרוטאוליטית מיטבית. Cathepsin K מסוגל להשפיל ג'לטין ב- pH 7 ו- 8, אך רמות ה- pH הללו אינן מאפשרות פעילות של Cathepsins L ו- V. ב- pH 4 קתפסין V פעיל, אך קתפסין K אינו פעיל. התאמת ה- pH של חיץ ההפעלה יכולה לאפשר זיהוי נוסף של סוגי קתפסין.[20]
הִיסטוֹרִיָה
המונח קתפסין הוטבע בשנת 1929 על ידי ריצ'רד ווילשטטר ו- Eugen Bamann לתאר פעילות פרוטאוליטית של לויקוציטים ורקמות ב- pH מעט חומצי (Willstätter & Bamann (1929) Hoppe-Seylers Z. Physiol. Chemie 180, 127-143). התיעוד המוקדם ביותר של "קתפסין" שנמצא ב MEDLINE מסד נתונים (למשל באמצעות PubMed ) הוא מה כתב העת לכימיה ביולוגית בשנת 1949.[21] עם זאת, התייחסויות במאמר זה מצביעות על כך שזוהו תחילה קתפסינים ושמו סביב תחילת המאה העשרים. חלק ניכר מעבודות קודמות אלה נעשה במעבדה של מקס ברגמן, שבילה את העשורים הראשונים של המאה בהגדרת פרוטאזות אלה.[22]
ראוי לציין כי מחקרים שפורסמו בשנות השלושים (בעיקר על ידי ברגמן) השתמשו במונח "אנזימים קתפטיים" כדי להתייחס למשפחה רחבה של פרוטאזות שכללה פפאין, ברומלין וקתפסין עצמו.[23] המאמצים הראשוניים לטהר ולאפיין פרוטאזות באמצעות המוגלובין התרחשו בזמן שהמילה "קתפסין" הצביעה על אנזים יחיד;[24] נראה כי לא ניתן היה להבין את קיומם של בני משפחת קתפסין מרובים (למשל B, H, L). עם זאת, בשנת 1937 ברגמן ועמיתיו החלו להבדיל בין קתפסינים על בסיס מקורם בגוף האדם (למשל קתפסין כבד, קתפסין טחול).[22]
הפניות
- ^ א ב Nomura T, Katunuma N (פברואר 2005). "מעורבות קתפסינים בפלישה, גרורות וריבוי תאים סרטניים" (PDF). ג'יי מד. להשקיע. 52 (1–2): 1–9. דוי:10.2152 / jmi.52.1. PMID 15751268.
- ^ ליפטון פ '(אוקטובר 1999). "מוות של תאים איסכמיים בנוירונים במוח". פיסיול. לְהַאִיץ. 79 (4): 1431–568. דוי:10.1152 / physrev.1999.79.4.1431. PMID 10508238.
- ^ Xu J, Wang H, Ding K, Lu X, Li T, Wang J, Wang C, Wang J (24 באוקטובר 2013). "עיכוב קתפסין S מייצר השפעות נוירו-מגן לאחר פגיעה מוחית טראומטית בעכברים". מתווכי דלקת. 2013 (2013): 187873. דוי:10.1155/2013/187873. PMC 3824312. PMID 24282339.
- ^ ימשימה טי (2013). "שקול מחדש את מחלת אלצהיימר על ידי 'השערת קלפין-קתפסין' - סקירה פרספקטיבית". התקדמות בנוירולוגיה. 105: 1–23. דוי:10.1016 / j.pneurobio.2013.02.004. PMID 23499711. S2CID 39292302.
- ^ Raptis SZ, שפירו SD, ראש הממשלה סימונס, צ'נג AM, Pham CT (יוני 2005). "סרין פרוטאז קתפסין G מווסת את תפקודי אפקט הנויטרופילים התלויים בהידבקות על ידי ויסות אשכולות אינטגרין". חֲסִינוּת. 22 (6): 679–91. דוי:10.1016 / j.immuni.2005.03.015. PMID 15963783.
- ^ Chandran K (2005). "חלבון אנדוזומלי של נגיף האבולה גליקופרוטאין הכרחי להדבקה". מַדָע. 308 (5728): 1643–1645. ביבקוד:2005Sci ... 308.1643C. דוי:10.1126 / science.1110656. PMC 4797943. PMID 15831716.
- ^ Im E, Kazlauskas A (מרץ 2007). "תפקיד הקתפסינים בפיזיולוגיה ופתולוגיה של העין". תאריך תפוגה Res Res. 84 (3): 383–8. דוי:10.1016 / j.exer.2006.05.017. PMID 16893541.
- ^ הוק, גרגורי; הוק, ויויאן; קינדי, מארק (01-01-2011). "מעכב הפרוסטאז של ציסטאין, E64d, מפחית עמילואיד- β במוח ומשפר את ליקויי הזיכרון במודלים של בעלי חיים במחלת אלצהיימר על ידי עיכוב קתפסין B, אך לא פעילות BACE1, β-secretase".. כתב העת למחלת אלצהיימר. 26 (2): 387–408. דוי:10.3233 / JAD-2011-110101. ISSN 1875-8908. PMC 4317342. PMID 21613740.
- ^ חביבאללהי, פיימן; פיגירדו, חוסה-לואיז; היידארי, פדרם; דולאק, אוסטין M; אימאמורה, יו; בס, אדם י. אוגינו, שוג'י; צ'אן, אנדרו טי; מחמוד, עומר (2012). "הדמיה אופטית עם בדיקה מופעלת של קתפסין B לזיהוי משופר של אדנוקרצינומה הוושט על ידי אנדוסקופיה GI עליונה פלואורסצנטית עם ערוץ כפול". תרנוסטיקה. 2 (2): 227–234. דוי:10.7150 / thno.4088. PMC 3296470. PMID 22400064.
- ^ לקידר M, קסטינו R, Bouguyon E, Isidoro C, Ollivier-Bousquet M (2004). "קתפסין D המשוחרר על ידי תאי אפיתל החלב של חולדה מניקה מעורב במחשוף פרולקטין בתנאים פיזיולוגיים.". כתב העת למדעי התא. 117 (נק '21): 5155-5164. דוי:10.1242 / jcs.01396. PMID 15456852.
- ^ שי GP, צ'פמן HA, בהאירי SM, DeLeeuw C, Reddy VY, Weiss SJ (ינואר 1995). "שיבוט מולקולרי של קתפסין O אנושי, אנדופרוטיינאז חדש והומולוג של ארנב OC2" (PDF). FEBS לט. 357 (2): 129–34. דוי:10.1016/0014-5793(94)01349-6. hdl:2027.42/116965. PMID 7805878. S2CID 28099876.
- ^ Gocheva V, Joyce JA (ינואר 2007). "ציסטאין קתפסינים וחוד החנית של פלישת סרטן". מחזור תאים. 6 (1): 60–4. דוי:10.4161 / cc.6.1.3669. PMID 17245112.
- ^ לוטג'נס E, לוטג'נס SP, פבר לפני הספירה, היינמן S, ג'יבלס מ.מ., דה ווינטר פרלמנט, פרדריק P, ואן דר מייד I, Daugherty A, Sijbers AM, Fisher A, Long CJ, Saftig P, Black D, Daemen MJ, Cleutjens KB (ינואר 2006). "הפרעה בגן קתפסין K מפחיתה את התקדמות טרשת העורקים ומשרה פיברוזיס של פלאק אך מאיצה את היווצרות תאי קצף מקרופאג". מחזור. 113 (1): 98–107. דוי:10.1161 / CIRCULATIONAHA.105.561449. PMID 16365196.
- ^ Platt MO, Ankeny RF, Shi GP, Weiss D, Vega JD, Taylor WR, Jo H (מרץ 2007). "ביטוי של קתפסין K מווסת על ידי מתח גזירה בתאי אנדותל מתורבת ומוגבר באנדותל בטרשת עורקים אנושית". אמ. ג'י פיסיול. לב לב. פיסיול. 292 (3): H1479–86. דוי:10.1152 / ajpheart.00954.2006. PMID 17098827.
- ^ סלמינן-מנקונן HJ, Morko J, Vuorio E (פברואר 2007). "תפקיד הקתפסין K במפרקים תקינים ובפיתוח דלקת פרקים". יעדי סמים. 8 (2): 315–23. דוי:10.2174/138945007779940188. PMID 17305509.
- ^ Brömme D, Li Z, Barnes M, Meler E (פברואר 1999). "ביטוי תפקודי של קתפסין V אנושי, חלוקת רקמות, פוטנציאל פני שטח אלקטרוסטטי, אפיון אנזימטי ולוקליזציה כרומוזומלית". בִּיוֹכִימִיָה. 38 (8): 2377–85. דוי:10.1021 / bi982175f. PMID 10029531.
- ^ יאנג M, ג'אנג Y, Pan J, Sun J, Liu J, Libby P, Sukhova GK, Doria A, Katunuma N, Peroni OD, Guerre-Millo M, Kahn BB, Clement K, Shi GP (אוגוסט 2007). "פעילות Cathepsin L שולטת באדיפוגנזה וסובלנות לגלוקוז". נט. תאי ביול. 9 (8): 970–7. דוי:10.1038 / ncb1623. PMC 3065497. PMID 17643114.
- ^ Bratkovič, et al. (2005). "בחירת זיקה לפפאין מניבה מעכבי פפטיד חזקים של קתפסינים L, B, H ו- K.". תקשורת מחקרית ביוכימית וביופיזית. 332 (3): 897–903. דוי:10.1016 / j.bbrc.2005.05.028. PMID 15913550.
- ^ א ב Li WA, Bar ZT, Cohen JD, Wilder CL, Deeds RJ, Keegan PM, Platt MO (יוני 2010). "איתור כמויות פמטומול של קתפסין K בוגר עם צימוגרפיה". אנאלי. ביוכם. 401 (1): 91–8. דוי:10.1016 / j.ab.2010.02.035. PMID 20206119.
- ^ ווילדר CL, פארק KY, ראש ממשלת קיגן, פלאט MO (דצמבר 2011). "מניפולציה של מצע ו- pH בפרוטוקולי הזימוגרפיה מבדילה באופן סלקטיבי את פעילות הקתפסינים K, L, S ו- V בתאים וברקמות". קֶשֶׁת. ביוכם. ביופיז. 516 (1): 52–7. דוי:10.1016 / j.abb.2011.09.009. PMC 3221864. PMID 21982919.
- ^ Maver ME, Greco AE (דצמבר 1949). "הידרוליזה של נוקלאופרוטאינים על ידי קתפסינים מתימוס עגל". ג'יי ביול. כימיה. 181 (2): 853–60. PMID 15393803.
- ^ א ב ברגמן M, פרוטון JS (יולי 1936). "לגבי האופי הכללי של אנזימים קתפטיים". מַדָע. 84 (2169): 89–90. ביבקוד:1936Sci .... 84 ... 89 ב. דוי:10.1126 / science.84.2169.89. PMID 17748131.
- ^ ברגמן M, פרוטון JS (1 ביוני 1937). "על אנזימים פרוטאוליטיים XV. לגבי האופי הכללי של אנזימים פרוטאוליטיים תאיים". כתב העת לכימיה ביולוגית. 119: 35–46.
- ^ אנסון, מ 'ל' (ספטמבר 1936). "הערכת קתפסין עם המוגלובין וטיהור חלקי של קתפסין". כתב העת לפיזיולוגיה כללית. 20 (4): 565–574. דוי:10.1085 / jgp.20.4.565. PMC 2141516. PMID 19873011.
קישורים חיצוניים
- ה MEROPS מסד נתונים מקוון לפפטידזים ומעכביהם: A01.010
- Cathepsins בספרייה הלאומית לרפואה בארה"ב כותרות נושא רפואי (רֶשֶׁת)
