חומצה ריבונוקלאית (RNA) הוא פולימרי מולקולה חיונית בתפקידים ביולוגיים שונים ב סִמוּל, פִּעַנוּחַ, תַקָנָה ו ביטוי שֶׁל גנים. RNA ו- DNA הם חומצות גרעין. ביחד עם ליפידים, חלבונים, ו פחמימות, חומצות גרעין מהוות אחת מארבע הגדולות מקרומולקולות חיוני לכל הצורות הידועות של חַיִים. כמו DNA, ה- RNA מורכב כשרשרת של נוקלאוטידים, אך בניגוד ל- DNA, RNA נמצא בטבע כחוט בודד המקופל על עצמו, ולא כחוט כפול זוגי. אורגניזמים סלולריים משתמשים שליח RNA (mRNAלהעביר מידע גנטי (באמצעות בסיסים חנקניים שֶׁל גואנין, אורציל, אדנין, ו ציטוזין, מסומן באותיות G, U, A ו- C) המכוון סינתזה של חלבונים ספציפיים. רב וירוסים לקודד את המידע הגנטי שלהם באמצעות RNA גנום.
חלק ממולקולות ה- RNA ממלאות תפקיד פעיל בתאים על ידי זרז תגובות ביולוגיות, שליטה ביטוי גנים, או חישה ותקשורת של תגובות לאותות הסלולר. אחד התהליכים הפעילים הללו הוא סינתזת חלבונים, פונקציה אוניברסלית בה מולקולות RNA מכוונות את סינתזת החלבונים הלאה ריבוזומים. תהליך זה משתמש העברת RNA (tRNA) מולקולות להעביר חומצות אמינו לריבוזום, איפה RNA ריבוזומלי (rRNAואז מקשר בין חומצות אמינו ליצירת חלבונים מקודדים.
השוואה עם DNA
כמו DNA, רוב ה- RNA הפעילים ביולוגית, כולל mRNA, tRNA, rRNA, snRNAs, ואחר RNAs שאינם מקודדים, מכילים רצפים המשלימים את עצמם המאפשרים לחלקים של ה- RNA להתקפל[5] ולהשתלב עם עצמו כדי ליצור סלילים כפולים. ניתוח של RNAs זה גילה שהם מאוד מובנים. בניגוד ל- DNA, המבנים שלהם אינם מורכבים מסלילים כפולים ארוכים, אלא מאוספים של סלילים קצרים שנארזים יחד למבנים הדומים לחלבונים.
באופן זה, RNAs יכולים להשיג כימיקלים קָטָלִיזָה (כמו אנזימים).[6] למשל, קביעת מבנה הריבוזום - קומפלקס RNA-חלבון המזרז יצירת קשרי פפטיד - העלתה שהאתר הפעיל שלו מורכב כולו מ- RNA.[7]
מִבְנֶה

כל אחד נוקלאוטיד ב- RNA מכיל a ריבוז סוכר, עם פחמנים שמספרם 1 'עד 5'. בסיס מחובר למצב 1 ', באופן כללי, אדנין (א), ציטוזין (ג), גואנין (G), או אורציל (U). אדנין וגואנין הם פורינים, ציטוזין ואורציל הם פירימידינים. א פוֹספָט הקבוצה מחוברת למצב 3 'של ריבוז אחד ולמיקום 5' של הבא. לקבוצות הפוספטים יש מטען שלילי כל אחד, מה שהופך את ה- RNA למולקולה טעונה (פוליאניון). הבסיסים נוצרים קשרי מימן בין ציטוזין לגואנין, בין אדנין לאוראציל ובין גואנין לאוראציל.[8] עם זאת, אינטראקציות אחרות אפשריות, כגון קבוצה של בסיסי אדנין המחייבים זה את זה בבליטה,[9]או ה- GNRA tetraloop שיש לו בסיס בסיס גואנין – אדנין.[8]
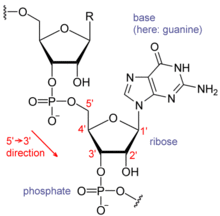
מרכיב מבני חשוב של RNA המבדיל אותו מ- DNA הוא נוכחותו של a הידרוקסיל קבוצה במצב 2 'של סוכר הריבוז. נוכחותה של קבוצה פונקציונאלית זו גורמת לסליל לקחת בעיקר את גיאומטריה בצורת A,[10] אם כי בהקשרים של דינוקלאוטידים חד גדילים, RNA לעתים רחוקות יכול גם לאמץ את צורת ה- B הנפוצה ביותר ב- DNA.[11] הגיאומטריה של צורת ה- A מביאה לחריץ ראשי עמוק וצר וחריץ מינורי רדוד ורחב.[12] תוצאה שנייה של נוכחות קבוצת 2'-הידרוקסיל היא שבאזורים גמישים קונפורמציהיים של מולקולת RNA (כלומר, לא מעורב ביצירת סליל כפול), היא יכולה לתקוף כימית את הקשר הפוספודיאסטר הסמוך כדי לנתק את עמוד השדרה.[13]

RNA מועתק עם ארבעה בסיסים בלבד (אדנין, ציטוזין, גואנין ואורציל),[14] אך ניתן לשנות את הבסיסים והסוכרים המצורפים בדרכים רבות עם התבגרות ה- RNA. פסאודורידין (Ψ), שבו הקשר בין אורציל לריבוז משתנה מקשר C – N לקשר C – C, ו ריבוטימידין (T) נמצאים במקומות שונים (הבולטים שבהם נמצאים בלולאת TΨC של tRNA ).[15] בסיס שונה בולט נוסף הוא היפוקסנטין, בסיס אדנין דיאמי אשר נוקלאוזיד נקרא אינוזין (אני). אינוזין ממלא תפקיד מפתח ב השערה מתנדנדת של ה קוד גנטי.[16]
ישנם יותר מ -100 נוקלאוזידים מהונדסים באופן טבעי.[17] ניתן למצוא את המגוון המבני הגדול ביותר של שינויים tRNA,[18] ואילו פסאודורידין ונוקלאוזידים עם 2'-O-methylribose לרוב נמצאים ב- rRNA הם הנפוצים ביותר.[19] התפקידים הספציפיים של רבים מהשינויים הללו ב- RNA אינם מובנים במלואם. עם זאת, ראוי לציין כי ב- RNA ריבוזומלי, רבים מהשינויים שלאחר תעתיק מתרחשים באזורים פונקציונליים במיוחד, כגון מרכז טרנספרז פפטידל וממשק יחידת המשנה, ומרמזים שהם חשובים לתפקוד תקין.[20]
הצורה הפונקציונלית של מולקולות RNA חד גדיליות, בדיוק כמו חלבונים, דורשת לעתים קרובות ספציפי מבנה שלישוני. הפיגום למבנה זה מסופק על ידי מבני משני יסודות שהם קשרי מימן בתוך המולקולה. זה מוביל למספר "תחומים" מוכרים של מבנה משני כמו לולאות סיכת ראש, בליטות, ו לולאות פנימיות.[21] מכיוון ש- RNA נטען, יונים מתכתיים כגון מג2+ נדרשים לייצוב רבים משניים ו מבנים שלישוניים.[22]
באופן טבעי אננטיומר של RNA הוא ד-RNA מורכב מ ד-ריבונוקליאוטידים. כל מרכזי הכיראליות נמצאים ב דשקט. על ידי שימוש ב ל-שקט או יותר נכון ל-ריבונוקליאוטידים, לניתן לסנתז את ה- RNA. ל-RNA יציב הרבה יותר נגד השפלה על ידי RNase.[23]
כמו ביו פולימרים מובנים אחרים כמו חלבונים, ניתן להגדיר טופולוגיה של מולקולת RNA מקופלת. זה נעשה לעתים קרובות על בסיס סידור של מגעים תוך שרשרת בתוך RNA מקופל, המכונה טופולוגיית מעגלים.
סִינתֶזָה
סינתזה של RNA בדרך כלל מזרזת אנזים -RNA פולימראז - שימוש ב- DNA כתבנית, תהליך המכונה תַעֲתוּק. התחלת שעתוק מתחילה בקשירת האנזים ל- a מְקַדֵם רצף ב- DNA (נמצא בדרך כלל "במעלה הזרם" של גן). הסליל הכפול של ה- DNA נפרש על ידי ה- הליקייס פעילות האנזים. לאחר מכן האנזים מתקדם לאורך גדיל התבנית בכיוון 3 'עד 5', ומסנתז מולקולת RNA משלימה עם התארכות בכיוון 5 'עד 3'. רצף ה- DNA מכתיב גם היכן תתרחש סיום סינתזת ה- RNA.[24]
תמליל ראשוני RNAs הם לעתים קרובות שונה על ידי אנזימים לאחר תעתיק. לדוגמא, א זנב פולי (A) ו מכסה 5 ' מתווספים לאוקריוטים טרום mRNA ו אינטרונים מוסרים על ידי אחוי.
יש גם מספר פולימראזות RNA תלויות RNA המשתמשים ב- RNA כתבנית שלהם לסינתזה של גדיל חדש של RNA. לדוגמא, מספר נגיפי רנ"א (כמו פוליווירוס) משתמשים באנזים מסוג זה כדי לשכפל את החומר הגנטי שלהם.[25] כמו כן, RNA פולימראז תלוי RNA הוא חלק מה- הפרעות RNA מסלול באורגניזמים רבים.[26]
סוגי RNA
סקירה כללית

שליח RNA (mRNA) הוא ה- RNA שמעביר מידע מ- DNA אל ה- ריבוזום, אתרי סינתזת החלבון (תִרגוּם ) בתא. רצף הקידוד של ה- mRNA קובע את חומצת אמינו רצף ב חֶלְבּוֹן שמופק.[27] עם זאת, RNAs רבים אינם מקודדים לחלבון (כ- 97% מתפוקת התעתיק אינה מקודדת חלבונים באאוקריוטים.[28][29][30][31]).
מה שנקרא RNAs שאינם מקודדים ("ncRNA") יכול להיות מקודד על ידי הגנים שלהם (גנים של RNA), אך יכול לנבוע גם מ- mRNA אינטרונים.[32] הדוגמאות הבולטות ביותר ל- RNA שאינם מקודדים הן העברת RNA (tRNA) ו- RNA ריבוזומלי (rRNA), שניהם מעורבים בתהליך התרגום.[4] ישנם גם RNAs שאינם מקודדים המעורבים בוויסות גנים, עיבוד RNA ותפקידים אחרים. RNAs מסוימים מסוגלים לזרז תגובות כימיות כגון חיתוך ו קשירה מולקולות RNA אחרות,[33] והזרז של קשר פפטיד היווצרות ב ריבוזום;[7] אלה ידועים בשם ריבוזימים.
באורך
על פי אורך שרשרת ה- RNA, ה- RNA כולל RNA קטן ו- RNA ארוך.[34] בְּדֶרֶך כְּלַל, RNA קטנים הם נמוכים מ- 200nt באורך, ורנ"א ארוכים גדולים מ- 200nt ארוך.[35] RNAs ארוכים, הנקראים גם RNAs גדולים, כוללים בעיקר RNA ארוך שאינו מקודד (lncRNA) ו- mRNA. RNAs קטנים כוללים בעיקר 5.8S RNA ריבוזומלי (rRNA), 5S rRNA, העברת RNA (tRNA), microRNA (מירנה), RNA מפריע קטן (siRNA), RNA גרעיני קטן (snoRNAs), RNA עם אינטראקציה פיווי (piRNA), RNA קטן הנגזר מ- tRNA (tsRNA)[36] ו- RNA קטן שמקורו ב- rDNA (srRNA).[37]ישנם חריגים מסוימים כמו במקרה של 5S rRNA של חברי הסוג הלוקוקוס (ארכאה ), שיש בהם הכנסה, ובכך מגדילים את גודלם.[38][39][40]
בתרגום
שליח RNA (mRNA) מביא מידע על רצף חלבונים אל ה- ריבוזומים, מפעלי סינתזת החלבון בתא. זה מקודד כך שכל שלושה נוקלאוטידים (א קודון ) תואם חומצת אמינו אחת. ב אוקריוטי לאחר תעתיק ה- DNA של קודמת ה- mRNA (טרום ה- mRNA), הוא מעובד ל- mRNA בוגר. זה מסיר את שלה אינטרונים -קטעים לא קידודיים של ה- pre-mRNA. ה- mRNA מיוצא לאחר מכן מהגרעין לציטופלזמה, שם הוא קשור לריבוזומים ו מְתוּרגָם לצורת החלבון המקבילה שלו בעזרת tRNA. בתאים פרוקריוטיים, שאין בהם תא גרעין וציטופלזמה, mRNA יכול להיקשר לריבוזומים בזמן שהוא מועתק מדנ"א. לאחר פרק זמן מסוים ההודעה מתפרקת לנוקליאוטידים המרכיבים אותה בעזרת ריבונוקליזות.[27]
העבר RNA (tRNA) היא שרשרת RNA קטנה של כ- 80 נוקלאוטידים המעבירה חומצת אמינו ספציפית לגידול פוליפפטיד שרשרת באתר הריבוזומלי של סינתזת החלבון במהלך התרגום. יש בו אתרים להצמדת חומצות אמינו ו אנטיקודון אזור עבור קודון זיהוי הנקשר לרצף ספציפי בשרשרת ה- RNA המסנג'ר באמצעות קשירת מימן.[32]
RNA ריבוזומלי (rRNA) הוא המרכיב הקטליטי של הריבוזומים. ריבוזומים אוקריוטיים מכילים ארבע מולקולות rRNA שונות: 18S, 5.8S, 28S ו- 5S rRNA. שלוש ממולקולות ה- rRNA מסונתזות ב גרעין, ואחד מסונתז במקום אחר. בציטופלזמה, ריבוזומלי RNA וחלבון משתלבים ויוצרים נוקלאופרוטאין הנקרא ריבוזום. הריבוזום קושר mRNA ומבצע סינתזת חלבון. ניתן לחבר מספר ריבוזומים ל- mRNA יחיד בכל עת.[27] כמעט כל ה- RNA שנמצא בתא אוקריוטי טיפוסי הוא rRNA.
העברת שליח RNA (tmRNA) נמצא אצל רבים בַּקטֶרִיָה ו פלסטידים. הוא מתייג חלבונים שמקודדים על ידי mRNA חסרים קודני עצירה לצורך השפלה ומונע את הריבוזום להיתקע.[41]
RNA רגולטורי
הרגולטורים המוקדמים ביותר הידועים של ביטוי גנים היו חלבונים המכונים מדכאים ו מפעילים, רגולטורים עם אתרי קישור קצרים ספציפיים בתוך משפר אזורים ליד הגנים שיש לווסת.[42] לאחרונה, נמצא כי RNAs מווסתים גם גנים. ישנם מספר סוגים של תהליכים תלויי RNA באיקריוטים המסדירים את ביטוי הגנים בנקודות שונות, כגון RNAi הדחקת גנים לאחר תמלול ברית, RNAים ארוכים שאינם מקודדים סגירת בלוקים של כרומטין באופן אפיגנטי, ו משפר RNAs גורם לביטוי גנים מוגבר.[43] בנוסף למנגנונים אלו באיקריוטים, נמצאו חיידקים וארכאות המשתמשים באופן נרחב ב- RNAs רגולטוריים. RNA קטן בקטריאלי וה CRISPR מערכת הן דוגמאות למערכות RNA רגולטוריות כאלה של פרוקריוטים.[44] אש ומלו הוענקו בשנת 2006 פרס נובל לפיזיולוגיה או לרפואה לגילוי מיקרו רנ"א (miRNAs), מולקולות RNA קצרות ספציפיות שיכולות להתבסס עם mRNAs.[45]
הפרעות RNA על ידי miRNAs
ניתן לשלוט על רמות ביטוי לאחר תעתיק של גנים רבים הפרעות RNA, שבו מירנה, מולקולות קצרות ספציפיות של RNA, התאימו לאזורי mRNA וכוונו אותם להתדרדרות.[46] זֶה אנטיסנס תהליך מבוסס כולל שלבים המעבדים תחילה את ה- RNA כך שהוא יכול זוג בסיס עם אזור של mRNAs היעד שלו. ברגע שהזיווג הבסיסי מתרחש, חלבונים אחרים מכוונים את ה- mRNA להשמדתו גרעינים.[43] אש ומלו הוענקו בשנת 2006 פרס נובל לפיזיולוגיה או לרפואה לתגלית זו.[45]
RNAים ארוכים שאינם מקודדים
הבאים להיות מקושרים לרגולציה היו קסיסט ואחר RNAים ארוכים שאינם מקודדים קשור ל אי-הפעלת כרומוזום X. תפקידיהם, בהתחלה מסתוריים, הוצגו על ידי ג'ני טי לי ואחרים להיות ה הַשׁתָקָה של גושי כרומטין באמצעות גיוס של Polycomb מורכב כך שלא ניתן היה לתמלל מהם RNA שליח.[47] LncRNA נוספים, המוגדרים כיום כ- RNA של יותר מ- 200 זוגות בסיס שלא נראה שיש להם פוטנציאל קידוד,[48] נמצאו קשורים לוויסות של תא גזע ריבוי יכולות ו חלוקת תא.[48]
משפר RNAs
הקבוצה העיקרית השלישית של RNAs רגולטוריים נקראת משפר RNAs.[48] כרגע לא ברור אם הם קטגוריה ייחודית של RNAs באורכים שונים או מהווים תת-קבוצה ברורה של lncRNAs. בכל מקרה, הם מתועתקים מ משפרי, שהם אתרי ויסות ידועים ב- DNA ליד גנים שהם מווסתים.[48][49] הם מווסתים את תמלול הגן / ים תחת שליטה במגבר שממנו הם מתועתקים.[48][50]
RNA מווסת בפרוקריוטים
בתחילה נחשב כי ה- RNA הרגולטורי הוא תופעה אוקריוטית, חלק מההסבר מדוע נראה כל כך הרבה יותר תעתיק באורגניזמים גבוהים ממה שנחזה. אך ברגע שהחוקרים החלו לחפש מווסתים אפשריים של RNA בחיידקים, הם הופיעו גם שם, שכונו RNA קטן (sRNA).[51][44] נכון לעכשיו, האופי הנמצא בכל מקום של מערכות לוויסות RNA של גנים נדון כתמיכה ב עולם ה- RNA תֵאוֹרִיָה.[43][52] רנ"א קטנים חיידקיים בדרך כלל פועל באמצעות אנטיסנס זיווג עם mRNA כדי לווסת את התרגום שלו למטה, בין אם על ידי השפעה על היציבות או על ידי השפעה על יכולת קשירת cis[43] ריבוס-מכשפות התגלו גם הם. הם פועלים ברצף הרגולציה של ה- RNA באופן אלוסטרי. הם משנים צורה כשהם נקשרים מטבוליטים כך שהם צוברים או מאבדים את היכולת לקשור כרומטין לוויסות הביטוי של גנים.[53][54]
בארכאה יש גם מערכות של RNA רגולטורי.[55] מערכת CRISPR, ששימשה לאחרונה לעריכת DNA באתרו, פועל באמצעות רנ"א רגולטוריים בארכיא ובחיידקים בכדי לספק הגנה מפני פולשים לנגיפים.[43][56]
בעיבוד RNA

RNAs רבים מעורבים בשינוי RNAs אחרים.אינטרונים הם שחבור מִתוֹך טרום mRNA על ידי spliceosomes, המכילים כמה RNA גרעיני קטן (snRNA),[4] או שהאינטרונים יכולים להיות ריבוזימים שנחבאים מעצמם.[57]ניתן לשנות את ה- RNA גם על ידי שינוי הנוקליאוטידים שלו לנוקלאוטידים שאינם א, ג, ז ו U ב eukaryotes, שינויים של נוקליאוטידים RNA מכוונים באופן כללי על ידי RNAs גרעינים קטנים (snoRNA; 60-300 nt),[32] נמצא ב גרעין ו גופי קוואל. snoRNAs מתקשרים עם אנזימים ומנחים אותם למקום על RNA על ידי התאמה בסיסית ל- RNA זה. אנזימים אלה מבצעים את שינוי הנוקליאוטידים. rRNAs ו- tRNAs משתנים בהרחבה, אך snRNAs ו- mRNAs יכולים גם להיות המטרה לשינוי בסיס.[58][59] ניתן גם למתיל RNA.[60][61]
גנום RNA
כמו DNA, RNA יכול לשאת מידע גנטי. נגיפי RNA יש גנום מורכב מ- RNA המקודד מספר חלבונים. הגנום הנגיפי משוכפל על ידי חלק מאותם חלבונים, בעוד שחלבונים אחרים מגנים על הגנום כאשר חלקיק הנגיף עובר לתא מארח חדש. וירואידים הם קבוצה אחרת של פתוגנים, אך הם מורכבים רק מ- RNA, אינם מקודדים שום חלבון ומשוכפלים על ידי פולימראז של תא צמח מארח.[62]
בתמלול הפוך
נגיפי תמלול הפוכים משכפלים את הגנום שלהם על ידי תמלול הפוך עותקי DNA מה- RNA שלהם; עותקי DNA אלה מועתקים לאחר מכן ל- RNA חדש. Retrotransposons מופץ גם על ידי העתקת DNA ו- RNA זה מזה,[63] ו טלומראז מכיל RNA המשמש כתבנית לבניית קצות הכרומוזומים האיקריוטיים.[64]
RNA חד-גדילי

RNA דו-גדילי (dsRNA) הוא RNA בעל שני גדילים משלימים, בדומה ל- DNA המצוי בכל התאים, אך עם החלפת תימין באוראסיל. dsRNA יוצר את החומר הגנטי של חלקם וירוסים (נגיפי RNA דו גדיליים ). RNA כפול גדילי, כגון RNA נגיפי או siRNA, יכול להפעיל הפרעות RNA ב אקריוטים, בנוסף ל אינטרפרון תגובה ב בעלי חוליות.[65][66][67][68]
RNA מעגלי
בסוף שנות השבעים הוצג כי קיים קוולנטי סגור יחיד, כלומר צורה מעגלית של RNA המובע בכל רחבי ממלכת החי והצומח (ראה circRNA ).[69] מחשבים ש- circRNAs נוצרים באמצעות תגובה "אחוי אחורי" שבו ה- אחוי מצטרף לתורם במורד הזרם לאתר אחוי קבלה במעלה הזרם. עד כה תפקודם של circRNAs אינו ידוע במידה רבה, אם כי עבור כמה דוגמאות הוכחה פעילות ספוגית של microRNA.
תגליות עיקריות בביולוגיה של RNA

מחקר על RNA הביא לתגליות ביולוגיות חשובות רבות ולפרסי נובל רבים. חומצות גרעין התגלו בשנת 1868 על ידי פרידריך מישר, שכינה את החומר 'נוקליין' מאז שנמצא ב גַרעִין.[70] מאוחר יותר התגלה כי תאים פרוקריוטיים, שאין להם גרעין, מכילים גם חומצות גרעין. תפקידו של ה- RNA בסינתזת החלבון נחשד כבר בשנת 1939.[71] סוורו אוצ'ואה זכה בשנת 1959 פרס נובל לרפואה (משותף עם ארתור קורנברג לאחר שגילה אנזים שיכול לסנתז RNA במעבדה.[72] עם זאת, האנזים שגילה אוצ'ואה (פוספורילאז פולינוקליאוטידי ) הוצג מאוחר יותר כאחראי על פירוק ה- RNA, ולא על סינתזת ה- RNA. בשנת 1956 אלכס ריץ 'ודיוויד דייויס הכלאו שני גדילים נפרדים של RNA ליצירת הגביש הראשון של ה- RNA שמבנהו יכול להיקבע על ידי קריסטלוגרפיה של רנטגן.[73]
הרצף של 77 הנוקלאוטידים של tRNA שמרים נמצא על ידי רוברט וו. הולי בשנת 1965,[74] מנצח הולי פרס נובל לרפואה 1968 (משותף עם הר גובינד חורנה ו מרשל נירנברג ).
בתחילת שנות השבעים, רטרו-וירוסים ו תעתיק הפוך התגלו, והראו לראשונה כי אנזימים יכולים להעתיק RNA ל- DNA (ההפך מהדרך הרגילה להעברת מידע גנטי). לעבודה זו, דייוויד בולטימור, רנאטו דולבקו ו הווארד תמין הוענק פרס נובל בשנת 1975. בשנת 1976, וולטר פירס וצוותו קבעו את רצף הנוקליאוטידים השלם הראשון של גנום של נגיף RNA, זה של בקטריופאג MS2.[75]
בשנת 1977, אינטרונים ו שחבור RNA התגלו גם בנגיפי יונקים וגם בגנים תאיים, וכתוצאה מכך נובל ל- 1993 פיליפ שארפ ו ריצ'רד רוברטס מולקולות RNA קטליטיות (ריבוזימים ) התגלו בתחילת שנות השמונים, מה שהוביל לפרס נובל לשנת 1989 תומאס צ'ך ו סידני אלטמן. בשנת 1990 הוא נמצא בשנת פטוניה שגנים שהוכנסו יכולים להשתיק גנים דומים משל הצמח, הידועים כיום כתוצאה מ הפרעות RNA.[76][77]
בערך באותו זמן, נקראים כעת RNAs באורך 22 nt מיקרו רנ"א, נמצאו שיש להם תפקיד ב- התפתחות שֶׁל C. elegans.[78]מחקרים על הפרעות לרנ"א זכו בפרס נובל אנדרו פייר ו קרייג מלו בשנת 2006, ונובל נוסף הוענק על מחקרים על תעתיק RNA ל- רוג'ר קורנברג באותה השנה. גילוי ה- RNA המווסתים של הגן הביא לניסיונות לפתח תרופות העשויות מ- RNA, כגון siRNA, להשתיק גנים.[79] נוסף על פרסי נובל שהוענקו למחקר בנושא RNA בשנת 2009, הוענק על הבהרת המבנה האטומי של הריבוזום לוונקי ראמקרישנן, טום שטייץ ועדה יונת.
רלוונטיות לכימיה פרוביוטיקה ואביוגנזה
בשנת 1968, קרל ווז שיערו ש- RNA עשוי להיות קטליטי והציע כי צורות החיים המוקדמות ביותר (מולקולות משכפלות את עצמן) היו יכולות להסתמך על RNA הן כדי לשאת מידע גנטי והן לזרז תגובות ביוכימיות - עולם ה- RNA.[80][81]
במרץ 2015 מורכב DNA ו- RNA נוקלאוטידים, כולל אורציל, ציטוזין ו תימין, על פי הדיווחים הוקמו במעבדה תחת חלל חיצון באמצעות כימיקלים למתחילים, כגון פירימידין, an תרכובת אורגנית נפוץ ב מטאוריטים. פירימידין, כאילו פחמימנים ארומטיים פולי-ציקליים (PAH), הוא אחד התרכובות העשירות ביותר בפחמן המצוי ב עוֹלָם וייתכן שנוצר ב ענקים אדומים או ב אבק בין כוכבי וענני גז.[82]
ראה גם
הפניות
- ^ "RNA: המולקולה הרב-תכליתית". אוניברסיטת יוטה. 2015.
- ^ "נוקליאוטידים וחומצות גרעין" (PDF). אוניברסיטת קליפורניה, לוס אנג'לס. הועבר לארכיון מ המקורי (PDF) בתאריך 23/09/2015. הוחזר 2015-08-26.
- ^ שוקלה RN (2014). ניתוח כרומוזומים. ISBN 978-93-84568-17-7.
- ^ א ב ג ברג JM, Tymoczko JL, Stryer L (2002). בִּיוֹכִימִיָה (מהדורה חמישית). WH פרימן ופלוגה. עמ '118–19, 781–808. ISBN 978-0-7167-4684-3. OCLC 179705944.
- ^ Tinoco I, Bustamante C (אוקטובר 1999). "איך RNA מתקפל". כתב העת לביולוגיה מולקולרית. 293 (2): 271–81. דוי:10.1006 / jmbi.1999.3001. PMID 10550208.
- ^ היגס PG (אוגוסט 2000). "מבנה משני RNA: היבטים פיזיים וחישוביים". ביקורות רבעוניות על ביופיזיקה. 33 (3): 199–253. דוי:10.1017 / S0033583500003620. PMID 11191843.
- ^ א ב ניסן פ ', הנסן ג'יי, באן נ', מור פב ', שטייץ ת"א (אוגוסט 2000). "הבסיס המבני של פעילות הריבוזום בסינתזת קשרי פפטיד". מַדָע. 289 (5481): 920–30. ביבקוד:2000Sci ... 289..920N. דוי:10.1126 / science.289.5481.920. PMID 10937990.
- ^ א ב לי ג'יי.סי, גוטל RR (דצמבר 2004). "מגוון של קונפורמציות זוג-בסיס והופעתן במבנה ה- rRNA ובמוטיבים המבניים של ה- RNA". כתב העת לביולוגיה מולקולרית. 344 (5): 1225–49. דוי:10.1016 / j.jmb.2004.09.072. PMID 15561141.
- ^ Barciszewski J, Frederic B, Clark C (1999). ביוכימיה RNA וביוטכנולוגיה. ספרינגר. עמ '73–87. ISBN 978-0-7923-5862-6. OCLC 52403776.
- ^ Salazar M, Fedoroff OY, Miller JM, Ribeiro NS, Reid BR (אפריל 1993). "גדיל ה- DNA בדופלקסים היברידיים של DNA. RNA אינו בצורת B ולא בצורת A בפתרון". בִּיוֹכִימִיָה. 32 (16): 4207–15. דוי:10.1021 / bi00067a007. PMID 7682844.
- ^ Sedova A, Banavali NK (פברואר 2016). "RNA מתקרב לצורת ה- B בהקשרים דינוקלאוטידיים מוערמים יחיד". ביו פולימרים. 105 (2): 65–82. דוי:10.1002 / bip.22750. PMID 26443416. S2CID 35949700.
- ^ הרמן טי, DJ של פאטל (מרץ 2000). "RNA בולט כמוטיבים אדריכליים והכרה". מִבְנֶה. 8 (3): R47-54. דוי:10.1016 / S0969-2126 (00) 00110-6. PMID 10745015.
- ^ מיקולה S, סטנמן E, Nurmi K, Yousefi-Salakdeh E, Strömberg R, Lönnberg H (1999). "מנגנון יון המתכת שמקדם מחשוף של קשרי RNA פוספודיאסטר כולל זרז חומצה כללי על ידי יון האקווה המתכתי ביציאת הקבוצה היוצאת". כתב העת של החברה הכימית, עסקאות פרקין 2 (8): 1619–26. דוי:10.1039 / a903691a.
- ^ ינקובסקי JA, Polak JM (1996). ניתוח גנים קליני ומניפולציה: כלים, טכניקות ופתרון בעיות. הוצאת אוניברסיטת קיימברידג '. עמ '14. ISBN 978-0-521-47896-0. OCLC 33838261.
- ^ יו ק. CD מורו (מאי 2001). "זיהוי של אלמנטים קריטיים בגזע הקולט tRNA ובלולאת T (Psi) C הדרושים לנגיף מסוג 1 של נגיף חסר חיסוני אנושי". כתב העת לווירולוגיה. 75 (10): 4902–6. דוי:10.1128 / JVI.75.10.4902-4906.2001. PMC 114245. PMID 11312362.
- ^ אליוט MS, טרווין RW (פברואר 1984). "ביוסינתזה של אינוזין בהעברת RNA על ידי הכנסת אנזימטית של היפוקסנטין". כתב העת לכימיה ביולוגית. 259 (4): 2407–10. PMID 6365911.
- ^ Cantara WA, Crain PF, Rozenski J, McCloskey JA, Harris KA, Zhang X, Vendeix FA, Fabris D, Agris PF (ינואר 2011). "מסד שינוי ה- RNA, RNAMDB: עדכון 2011". מחקר על חומצות גרעין. 39 (גיליון מסד נתונים): D195-201. דוי:10.1093 / nar / gkq1028. PMC 3013656. PMID 21071406.
- ^ סול ד, ראג'בנדרי יו (1995). TRNA: מבנה, ביוסינתזה ותפקוד. ASM Press. עמ ' 165. ISBN 978-1-55581-073-3. OCLC 183036381.
- ^ נשיקה T (יולי 2001). "שינוי פוסט תעתיק מונחה RNA גרעיני קטן של RNAs תאיים". כתב העת EMBO. 20 (14): 3617–22. דוי:10.1093 / emboj / 20.14.3617. PMC 125535. PMID 11447102.
- ^ קינג TH, ליו B, מקולי RR, פורנייה MJ (פברואר 2003). "מבנה ופעילות הריבוזום משתנה בתאים חסרי snoRNP היוצרים פסאודורידינים במרכז טרנספראז של פפטידל". תא מולקולרי. 11 (2): 425–35. דוי:10.1016 / S1097-2765 (03) 00040-6. PMID 12620230.
- ^ מתיוס DH, דיסני MD, צ'יילדס JL, שרדר SJ, צוקר M, טרנר DH (מאי 2004). "שילוב אילוצי שינוי כימי באלגוריתם תכנות דינמי לחיזוי מבנה משני של RNA". הליכים של האקדמיה הלאומית למדעים של ארצות הברית של אמריקה. 101 (19): 7287–92. ביבקוד:2004PNAS..101.7287M. דוי:10.1073 / pnas.0401799101. PMC 409911. PMID 15123812.
- ^ טאן ZJ, חן SJ (יולי 2008). "תלות במלח של יציבות סיכת ראש של חומצת גרעין". כתב עת ביופיזי. 95 (2): 738–52. ביבקוד:2008BpJ .... 95..738T. דוי:10.1529 / biophysj.108.131524. PMC 2440479. PMID 18424500.
- ^ ווטר א ', קלוסמן S (ינואר 2015). "הפיכת אוליגונוקליאוטידים עם תמונת מראה לתרופות: התפתחות התרופות של שפיגלמר (®)". גילוי סמים היום. 20 (1): 147–55. דוי:10.1016 / j.drudis.2014.09.004. PMID 25236655.
- ^ Nudler E, Gottesman ME (אוגוסט 2002). "סיום תמלול ואנטי סיום ב- E. coli". גנים לתאים. 7 (8): 755–68. דוי:10.1046 / j.1365-2443.2002.00563.x. PMID 12167155. S2CID 23191624.
- ^ הנסן JL, לונג AM, שולץ SC (אוגוסט 1997). "מבנה ה- RNA פולימראז תלוי ה- RNA של הפוליווירוס". מִבְנֶה. 5 (8): 1109–22. דוי:10.1016 / S0969-2126 (97) 00261-X. PMID 9309225.
- ^ אלקוויסט פ '(מאי 2002). "פולימראזות RNA תלויות RNA, נגיפים והשתקת RNA". מַדָע. 296 (5571): 1270–73. ביבקוד:2002Sci ... 296.1270A. דוי:10.1126 / science.1069132. PMID 12016304. S2CID 42526536.
- ^ א ב ג קופר GC, האוסמן רי (2004). התא: גישה מולקולרית (מהדורה שלישית). סינואר. עמ '261–76, 297, 339–44. ISBN 978-0-87893-214-6. OCLC 174924833.
- ^ Mattick JS, Gagen MJ (ספטמבר 2001). "האבולוציה של רשתות גנים מרובות משימות מבוקרות: תפקידם של אינטרונים ושל רנ"א אחרים שאינם מקודדים בפיתוח אורגניזמים מורכבים".. ביולוגיה מולקולרית ואבולוציה. 18 (9): 1611–30. דוי:10.1093 / oxfordjournals.molbev.a003951. PMID 11504843.
- ^ Mattick JS (נובמבר 2001). "רנ"א שאינם מקודדים: אדריכלי המורכבות האיקריוטית". דוחות EMBO. 2 (11): 986–91. דוי:10.1093 / דוחות אמבו / kve230. PMC 1084129. PMID 11713189.
- ^ Mattick JS (אוקטובר 2003). "מאתגר את הדוגמה: השכבה הנסתרת של רנ"א שאינם מקודדים חלבונים באורגניזמים מורכבים" (PDF). BioEssays. 25 (10): 930–39. CiteSeerX 10.1.1.476.7561. דוי:10.1002 / bies.10332. PMID 14505360. הועבר לארכיון מ המקורי (PDF) בתאריך 2009-03-06.
- ^ Mattick JS (אוקטובר 2004). "התוכנית הגנטית הנסתרת של אורגניזמים מורכבים". מדע אמריקאי. 291 (4): 60–67. ביבקוד:2004SciAm.291d..60M. דוי:10.1038 / מדעי אמריקאי 1004-60. PMID 15487671.[קישור מת ]
- ^ א ב ג וירטה וו (2006). כריית התמליל - שיטות ויישומים. שטוקהולם: בית הספר לביוטכנולוגיה, המכון המלכותי לטכנולוגיה. ISBN 978-91-7178-436-0. OCLC 185406288.
- ^ רוסי ג'יי ג'יי (יולי 2004). "אבחון ריבוזים מתבגר". כימיה וביולוגיה. 11 (7): 894–95. דוי:10.1016 / j.chembiol.2004.07.002. PMID 15271347.
- ^ Storz G (מאי 2002). "יקום מתרחב של רנ"א שאינם מקודדים". מַדָע. 296 (5571): 1260–63. ביבקוד:2002Sci ... 296.1260S. דוי:10.1126 / science.1072249. PMID 12016301. S2CID 35295924.
- ^ Fatica A, Bozzoni I (ינואר 2014). "RNAים ארוכים שאינם מקודדים: שחקנים חדשים בבידול ופיתוח תאים". סקירת טבע גנטיקה. 15 (1): 7–21. דוי:10.1038 / nrg3606. PMID 24296535. S2CID 12295847.[קישור מת קבוע ]
- ^ צ'ן ק ', יאן מ', קאו זי, לי X, ג'אנג Y, שי ג'י, ואח '. (ינואר 2016). "זרעונים של זרע תורמים לירושה בין דורית להפרעה מטבולית נרכשת" (PDF). מַדָע. 351 (6271): 397–400. ביבקוד:2016Sci ... 351..397C. דוי:10.1126 / science.aad7977. PMID 26721680. S2CID 21738301.
- ^ Wei H, Zhou B, Zhang F, Tu Y, Hu Y, Zhang B, Zhai Q (2013). "פרופיל וזיהוי של RNAs קטנים שמקורם ב- rDNA ותפקידיהם הביולוגיים הפוטנציאליים שלהם". PLOS ONE. 8 (2): e56842. ביבקוד:2013PLoSO ... 856842W. דוי:10.1371 / journal.pone.0056842. PMC 3572043. PMID 23418607.
- ^ Luehrsen KR, Nicholson DE, Eubanks DC, Fox GE (1981). "אר-אר-בקטריאלי 5S rRNA מכיל רצף הכנסה ארוך". טֶבַע. 293 (נק '12): 755-756. דוי:10.1099/00221287-145-12-3565. PMID 6169998.
- ^ סטן-לוטר H, מקגניטי TJ, לגאט A, דנר EB, גלייזר K, סטטר KO, Wanner G (1999). "זנים דומים מאוד של Halococcus salifodinae נמצאים במאגרי מלח פרמו-טריאסיים המופרדים גיאוגרפית". מִיקרוֹבִּיוֹלוֹגִיָה. 145 (נק '12): 3565–3574. דוי:10.1099/00221287-145-12-3565. PMID 10627054.
- ^ Tirumalai MR, Kaelber JT, Park DR, Tran Q, Fox GE (אוגוסט 2020). "ויזואליזציה של מיקרוסקופית קריו-אלקטרונים של החדרה גדולה ב- RNA הריבוזומלי 5S של הארכיאון ההלופילי במיוחד מורוקי הלוקוקוס". FEBS ביו פתוח. 10 (10): 1938–1946. דוי:10.1002/2211-5463.12962. PMC 7530397. PMID 32865340.
- ^ Gueneau de Novoa P, Williams KP (ינואר 2004). "אתר tmRNA: התפתחות רדוקטיבית של tmRNA בפלסטידים ובאנדוסימביוטים אחרים". מחקר על חומצות גרעין. 32 (גיליון מסד נתונים): D104–08. דוי:10.1093 / nar / gkh102. PMC 308836. PMID 14681369.
- ^ יעקב F, מונוד J (1961). "מנגנוני ויסות גנטיים בסינתזת חלבונים". כתב העת לביולוגיה מולקולרית. 3 (3): 318–56. דוי:10.1016 / s0022-2836 (61) 80072-7. PMID 13718526.
- ^ א ב ג ד ה מוריס K, מאטיק ג'יי (2014). "עליית ה- RNA הרגולטורי". סקירת טבע גנטיקה. 15 (6): 423–37. דוי:10.1038 / nrg3722. PMC 4314111. PMID 24776770.
- ^ א ב גוטסמן S (2005). "מיקרו לחיידקים: RNAs רגולטוריים שאינם מקודדים בחיידקים". מגמות בגנטיקה. 21 (7): 399–404. דוי:10.1016 / j.tig.2005.05.008. PMID 15913835.
- ^ א ב "פרס נובל לפיזיולוגיה או לרפואה 2006". Nobelprize.org. נובל מדיה AB 2014. אינטרנט. 6 באוגוסט 2018. http://www.nobelprize.org/nobel_prizes/medicine/laureates/2006
- ^ אש, ואח '. (1998). "הפרעה גנטית חזקה וספציפית על ידי RNA כפול גדילי ב- Ceanorhabditis elegans". טֶבַע. 391 (6669): 806–11. ביבקוד:1998 Natur.391..806F. דוי:10.1038/35888. PMID 9486653. S2CID 4355692.
- ^ Zhao J, Sun BK, Erwin JA, Song JJ, Lee JT (2008). "חלבונים פוליביים ממוקדים על ידי RNA חוזר קצר לכרומוזום X של העכבר". מַדָע. 322 (5902): 750–56. ביבקוד:2008Sci ... 322..750Z. דוי:10.1126 / science.1163045. PMC 2748911. PMID 18974356.
- ^ א ב ג ד ה Rinn JL, Chang HY (2012). "ויסות הגנום על ידי RNAs ארוכים שאינם מקודדים". אננו. הכומר ביוכם. 81: 1–25. דוי:10.1146 / annurev-biochem-051410-092902. PMC 3858397. PMID 22663078.
- ^ טאפט RJ, CD קפלן, סימונס סי, מאטיק JS (2009). "אבולוציה, ביוגנזה ותפקוד של ה- RNA הקשורים לאמרגן". מחזור תאים. 8 (15): 2332–38. דוי:10.4161 / cc.8.15.9154. PMID 19597344.
- ^ אורום UA, Derrien T, Beringer M, Gumireddy K, Gardini A, et al. (2010). "'RNAים ארוכים ללא קידוד עם תפקוד דמוי משפר בתאים אנושיים ". תָא. 143 (1): 46–58. דוי:10.1016 / j.cell.2010.09.001. PMC 4108080. PMID 20887892.
- ^ EGH Wagner, P Romby. (2015). "רנ"א קטנים בחיידקים ובארכאות: מי הם, מה הם עושים ואיך הם עושים זאת". התקדמות בגנטיקה (כרך 90, עמ '133–208).
- ^ J.W. נלסון, R. R. Breaker (2017) "השפה האבודה של עולם ה- RNA."Sci. אוֹת.10, eaam8812 1–11.
- ^ WC Winklef (2005). "ריבוסוויטצ'ים ותפקידם של RNAs ללא קידוד בבקרת חילוף החומרים החיידקית". Curr. דעה. כימיה. ביול. 9 (6): 594–602. דוי:10.1016 / j.cbpa.2005.09.016. PMID 16226486.
- ^ טאקר BJ, Breaker RR (2005). "ריבוס-מכשירים כמרכיבי בקרת גנים רב-תכליתיים". Curr. דעה. מבנה. ביול. 15 (3): 342–48. דוי:10.1016 / j.sbi.2005.05.003. PMID 15919195.
- ^ מוח'יקה FJ, Diez-Villasenor C, Soria E, Juez G (2000). "" "חשיבות ביולוגית של משפחה של חזרות על בסיס קבוע בגנום של ארכיא, חיידק ומיטוכונדריה". מול. מיקרוביול. 36 (1): 244–46. דוי:10.1046 / j.1365-2958.2000.01838.x. PMID 10760181. S2CID 22216574.
- ^ Brouns S, Jore MM, Lundgren M, Westra E, Slijkhuis R, Snijders A, Dickman M, Makarova K, Koonin E, Der Oost JV (2008). "RNA קטן של CRISPR מנחה הגנה אנטי-ויראלית בפרוקריוטים". מַדָע. 321 (5891): 960–64. ביבקוד:2008Sci ... 321..960B. דוי:10.1126 / science.1159689. PMC 5898235. PMID 18703739.
- ^ Steitz TA, Steitz JA (יולי 1993). "מנגנון כללי של שני מתכות-יונים ל- RNA קטליטי". הליכים של האקדמיה הלאומית למדעים של ארצות הברית של אמריקה. 90 (14): 6498–502. ביבקוד:1993PNAS ... 90.6498S. דוי:10.1073 / pnas.90.14.6498. PMC 46959. PMID 8341661.
- ^ זי ג'יי, ג'אנג מ ', ג'ואו טי, הואה X, טאנג ל', וו וו (ינואר 2007). "Sno / scaRNAbase: מאגר נתונים עבור RNAs גרעינים קטנים ו- RNA ספציפיים לגוף".. מחקר על חומצות גרעין. 35 (גיליון מסד נתונים): D183–87. דוי:10.1093 / nar / gkl873. PMC 1669756. PMID 17099227.
- ^ עומר AD, Ziesche S, Decatur WA, Fournier MJ, Dennis PP (מאי 2003). "מכונות לשינוי RNA בארכאות". מיקרוביולוגיה מולקולרית. 48 (3): 617–29. דוי:10.1046 / j.1365-2958.2003.03483.x. PMID 12694609. S2CID 20326977.
- ^ Cavaillé J, Nicoloso M, Bachellerie JP (אוקטובר 1996). "מתילציה ממוקדת של ריבוז של RNA in vivo מכוונת על ידי מדריכי RNA אנטי-חושים מותאמים". טֶבַע. 383 (6602): 732–35. ביבקוד:1996 Natur.383..732C. דוי:10.1038 / 383732a0. PMID 8878486. S2CID 4334683.
- ^ Kiss-László Z, Henry Y, Bachellerie JP, Caizergues-Ferrer M, Kiss T (יוני 1996). "מתילציה ריבוזית ספציפית לאתר של RNA preribosomal: פונקציה חדשה עבור RNAs גרעינים קטנים." תָא. 85 (7): 1077–88. דוי:10.1016 / S0092-8674 (00) 81308-2. PMID 8674114. S2CID 10418885.
- ^ דארוס JA, אלנה SF, פלורס R (יוני 2006). "וירואידים: חוט של אריאדנה למבוך ה- RNA". דוחות EMBO. 7 (6): 593–98. דוי:10.1038 / sj.embor.7400706. PMC 1479586. PMID 16741503.
- ^ Kalendar R, Vicient CM, Peleg O, Anamthawat-Jonsson K, Bolshoy A, Schulman AH (מרץ 2004). "נגזרות רטרוטרנספוזון גדולות: רטרלמנטים שופעים, שמורים אך לא אוטונומיים של שעורה וגנומים קשורים". גנטיקה. 166 (3): 1437–50. דוי:10.1534 / גנטיקה.166.3.1437. PMC 1470764. PMID 15082561.
- ^ פודלבסקי JD, Bley CJ, Omana RV, Qi X, Chen JJ (ינואר 2008). "מאגר הטלומראז". מחקר על חומצות גרעין. 36 (גיליון מסד נתונים): D339–43. דוי:10.1093 / nar / gkm700. PMC 2238860. PMID 18073191.
- ^ Blevins T, Rajeswaran R, Shivaprasad PV, Beknazariants D, Si-Ammour A, Park HS, Vazquez F, Robertson D, Meins F, Hohn T, Pooggin MM (2006). "ארבע תרכובות צמחיות מתווכות ביוגנזה של RNA קטן ויראלי והשתקה המושרה על ידי נגיף DNA". מחקר על חומצות גרעין. 34 (21): 6233–46. דוי:10.1093 / nar / gkl886. PMC 1669714. PMID 17090584.
- ^ ג'אנה ס ', צ'אקראבוטי ג', ננדי ס ', דב ג'יי קיי (נובמבר 2004). "הפרעות RNA: מטרות טיפוליות פוטנציאליות". מיקרוביולוגיה שימושית וביוטכנולוגיה. 65 (6): 649–57. דוי:10.1007 / s00253-004-1732-1. PMID 15372214. S2CID 20963666.
- ^ שולץ U, Kaspers B, Staeheli P (מאי 2004). "מערכת האינטרפרון של בעלי חוליות שאינם יונקים". אימונולוגיה התפתחותית והשוואתית. 28 (5): 499–508. דוי:10.1016 / j.dci.2003.09.009. PMID 15062646.
- ^ ווייטהד KA, דהלמן JE, לנגר RS, אנדרסון DG (2011). "השתקה או גירוי? מסירת siRNA ומערכת החיסון". סקירה שנתית של הנדסה כימית וביו-מולקולרית. 2: 77–96. דוי:10.1146 / annurev-chembioeng-061010-114133. PMID 22432611.
- ^ Hsu MT, קוקה-פראדוס M (יולי 1979). "עדויות מיקרוסקופיות אלקטרוניות לצורה העגולה של RNA בציטופלזמה של תאים אוקריוטים". טֶבַע. 280 (5720): 339–40. ביבקוד:1979 Natur.280..339H. דוי:10.1038 / 280339a0. PMID 460409. S2CID 19968869.
- ^ דהם ר '(פברואר 2005). "פרידריך מישר וגילוי ה- DNA". ביולוגיה התפתחותית. 278 (2): 274–88. דוי:10.1016 / j.ydbio.2004.11.028. PMID 15680349.
- ^ קספרסון T, שולץ J (1939). "נוקלאוטידים של פנטוזה בציטופלזמה של רקמות צומחות". טֶבַע. 143 (3623): 602–03. ביבקוד:1939. Natur.143..602C. דוי:10.1038 / 143602c0. S2CID 4140563.
- ^ Ochoa S (1959). "סינתזה אנזימטית של חומצה ריבונוקלאית" (PDF). הרצאת נובל.
- ^ ריץ 'א', דייויס ד '(1956). "מבנה סלילי דו-גדילי חדש: חומצה פוליאדינלית וחומצה פוליאורידית". כתב העת של האגודה האמריקנית לכימיה. 78 (14): 3548–49. דוי:10.1021 / ja01595a086.
- ^ Holley RW, et al. (מרץ 1965). "מבנה של חומצה ריבונוקלאית". מַדָע. 147 (3664): 1462–65. ביבקוד:1965Sci ... 147.1462H. דוי:10.1126 / science.147.3664.1462. PMID 14263761. S2CID 40989800.
- ^ Fiers W, et al. (אפריל 1976). "רצף נוקלאוטיד מלא של חיידק MS2 RNA: מבנה ראשוני ומשני של הגן המשוכפל". טֶבַע. 260 (5551): 500–07. ביבקוד:1976 נאטור 260..500F. דוי:10.1038 / 260500a0. PMID 1264203. S2CID 4289674.
- ^ נאפולי C, Lemieux C, Jorgensen R (אפריל 1990). "הכנסת גן סינטזה כלקוני כימרי לפטוניה גורם לדיכוי הפיך משותף של גנים הומולוגיים בטרנס". תא הצמחים. 2 (4): 279–89. דוי:10.1105 / tpc.2.4.279. PMC 159885. PMID 12354959.
- ^ Dafny-Yelin M, Chung SM, Frankman EL, Tzfira T (דצמבר 2007). "וקטורי הפרעה של pSAT RNA: סדרה מודולרית לויסות מרובה של גן למטה בצמחים". פיזיולוגיית הצמח. 145 (4): 1272–81. דוי:10.1104 / עמ '107.106062. PMC 2151715. PMID 17766396.
- ^ Ruvkun G (אוקטובר 2001). "ביולוגיה מולקולרית. הצצות של עולם RNA זעיר". מַדָע. 294 (5543): 797–99. דוי:10.1126 / science.1066315. PMID 11679654. S2CID 83506718.
- ^ פיצ'ו י, פרץ ג '(דצמבר 2006). "הפוטנציאל של אוליגונוקליאוטידים ליישומים טיפוליים". מגמות בתחום הביוטכנולוגיה. 24 (12): 563–70. דוי:10.1016 / j.tibtech.2006.10.003. PMID 17045686.
- ^ סיברט S (2006). "מאפייני מבנה רצף משותף ואזורים יציבים במבנים משניים של RNA" (PDF). עבודת גמר, אלברט-לודוויגס-אוניברסיטה, פרייבורג אים ברייסגאו. עמ ' 1. הועבר לארכיון מ המקורי (PDF) ב- 9 במרץ 2012.
- ^ Szathmáry E (יוני 1999). "מקורו של הצופן הגנטי: חומצות אמינו כמקורות גורמים בעולם ה- RNA". מגמות בגנטיקה. 15 (6): 223–29. דוי:10.1016 / S0168-9525 (99) 01730-8. PMID 10354582.
- ^ מרלייר R (3 במרץ 2015). "איימס של נאס"א משחזרת את אבני החיים במעבדה". נאס"א. הוחזר 5 במרץ 2015.
קישורים חיצוניים
- אתר RNA World אוסף קישורים (מבנים, רצפים, כלים, כתבי עת)
- מאגר חומצות גרעין תמונות של DNA, RNA ומתחמים.
- הסמינר של אנה מארי פייל: מבנה RNA, פונקציה והכרה