| הַדבָּקָה | |
|---|---|
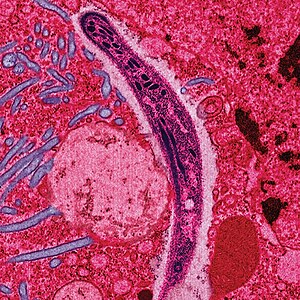 | |
| בצבע כוזב מיקרוגרף אלקטרונים מראה א מָלַרִיָה ספרוזואיט נודדים דרך אמצע אפיתל של א עכברוש | |
| תחום התמחות | מחלה מדבקת |
| סיבות | חיידקי, נְגִיפִי, טפילית, פטרייתי |
An הַדבָּקָה היא הפלישה לגוף של אורגניזם רקמות על ידי גורמים גורמים למחלות, הכפל שלהם, והתגובה של מנחה רקמות לגורמים המדבקים ול- רעלים הם מייצרים.[1][2] An מחלה מדבקת, המכונה גם א מחלה מועברת אוֹ מחלה מדבקת, הוא מחלה כתוצאה מזיהום.
זיהומים נגרמים על ידי גורמים זיהומיים (פתוגנים ) כולל:
- וירוסים וסוכנים קשורים כגון וירואידים (HIV, נגיף האף, ליסווירוסים כמו נגיף כלבת, וירוס אבולה ו תסמונת נשימה חריפה חמורה של קורונה )
- בַּקטֶרִיָה (שחפת מיקובקטריום, סטפילוקוקוס אוראוס, אי קולי, קלוסטרידיום בוטולינום, ו סלמונלה spp.)
- פטריות, מסווג משנה נוספת ל:
- Ascomycota, כולל שמרים כגון קִמָחוֹן, פטריות נימה כגון אספרגילוס, פנאומוציסטיס מינים, ו דרמטופיטים, קבוצה של אורגניזמים הגורמים לזיהום בעור ובמבנים שטחיים אחרים בבני אדם.[3]
- Basidiomycota, כולל הסוג האנושי-פתוגני קריפטוקוקוס.[4]
- פריונים (למרות שהם לא מפרישים רעלים)
- טפילים, המחולקים בדרך כלל ל:[5]
- אורגניזמים חד תאיים (למשל מָלַרִיָה, טוקסופלזמה, בבסיה )
- מקרופראזיטים[6] (תולעים או קסמי חן ) כולל נמטודות כמו טפילית תולעים עגולות ו תולעי סיכה, תולעי סרט (cestodes), ו flukes (trematodes, כגון סכיסטוזומיאזיס )
- פרוקי רגליים כמו קרציות, קרדית, פרעושים, ו כִּנִים, יכול גם לגרום למחלות אנושיות, אשר מבחינה מושגית דומות לזיהומים, אך בדרך כלל מכנים פלישה לגוף אנושי או בעל חיים על ידי מקרופראזיטים אלה שְׁרִיצָה. (מחלות הנגרמות על ידי helminths, שהם גם מקרופרזיטים, מכונים לפעמים גם נגיעות, אך לפעמים מכונים זיהומים.)
מארחים יכולים להילחם בזיהומים באמצעות שלהם מערכת החיסון. יונק מארחים מגיבים לזיהומים עם מוּטבָּע תגובה, מעורבת לעיתים קרובות דַלֶקֶת, ואחריו אדפטיבי תְגוּבָה.[7]
ספֵּצִיפִי תרופות המשמשים לטיפול בזיהומים כוללים אַנְטִיבִּיוֹטִיקָה, אנטי-וירליות, אנטי פטרייתי, אנטי פרוטוזואלים, ו אנטי-מינמיסטים. מחלות זיהומיות הביאו ל- 9.2 מיליון מקרי מוות בשנת 2013 (כ- 17% מכלל מקרי המוות).[8] הענף של תרופה המתמקד בזיהומים מכונה מחלה מדבקת.[9]
מִיוּן
תת קליני לעומת קליני (סמוי לעומת לכאורה)
זיהומים סימפטומטיים הם נִרְאֶה ו קליניואילו זיהום פעיל אך אינו מייצר תסמינים ניכרים לא נראה שקט, תת קליני, או נִסתָר. זיהום שאינו פעיל או רדום נקרא a זיהום סמוי.[10] דוגמא לזיהום חיידקי סמוי הוא שחפת סמויה. כמה זיהומים נגיפיים יכולים להיות גם סמויים, דוגמאות ל זיהומים נגיפיים סמויים האם כל אלה מאלה הרפסווירידים מִשׁפָּחָה.[11]
המילה הַדבָּקָה פחית לציין כל נוכחות של פתוגן מסוים בכלל (לא משנה כמה מעט) אך גם משמשת לעתים קרובות ב- לָחוּשׁ רומז א ניכר מבחינה קלינית זיהום (במילים אחרות, מקרה של מחלה זיהומית).[12] עובדה זו יוצרת מדי פעם כמה דו משמעות או מבקש כמה נוֹהָג דִיוּן; כדי לעקוף את זה זה נפוץ מומחי בריאות לדבר עליו קולוניזציה (ולא הַדבָּקָהכאשר הם מתכוונים לכך שחלק מהפתוגנים קיימים אך אין זיהום קליני (ללא מחלה).
מונחים שונים משמשים לתיאור זיהומים. הראשון הוא זיהום חריף. זיהום חריף הוא אחד שבו התסמינים מתפתחים במהירות; מהלכו יכול להיות מהיר או ממושך.[13] הבא הוא זיהום כרוני. זיהום כרוני הוא כאשר הסימפטומים מתפתחים בהדרגה, לאורך שבועות או חודשים, ואיטיים להיפתר.[14] זיהום תת-אקוטי הוא אחד שבו התסמינים לוקחים זמן רב יותר מאשר בזיהום חריף אך מתעוררים מהר יותר מזיהום כרוני. זיהום סמוי הוא סוג של זיהום שעלול להתרחש לאחר פרק חריף; האורגניזם קיים אך הסימפטומים אינם; לאחר זמן המחלה יכולה להופיע מחדש. זיהום מוקדי מוגדר כמקום ההדבקה הראשוני ממנו אורגניזמים עוברים דרך זרם הדם לאזור אחר בגוף.[15]
ראשוני מול אופורטוניסטי
בין שלל הזנים של מיקרואורגניזמים, מעטים יחסית גורמים למחלות אצל אנשים בריאים אחרת.[16] מחלה זיהומית נובעת מהמשחק בין מעטים אלה פתוגנים והגנות המארחים שהם מדביקים. המראה והחומרה של המחלה הנובעים מכל פתוגן תלוי ביכולתו של אותו פתוגן לפגוע במארח וכן ביכולתו של המארח להתנגד לפתוגן. עם זאת, מערכת החיסון של המארח עלולה גם לגרום נזק למארח עצמו בניסיון לשלוט בזיהום. לפיכך, רופאים מסווגים מיקרואורגניזמים או חיידקים מדבקים על פי מצב ההגנה המארחת - או כ- פתוגנים ראשוניים או כמו פתוגנים אופורטוניסטיים:
פתוגנים ראשוניים
פתוגנים ראשוניים גורמים למחלות כתוצאה מנוכחותם או מפעילותם בתוך המארח הרגיל והבריא ומהפנימיותם אַרסִיוּת (חומרת המחלה שהם גורמים) היא, בחלקה, תוצאה הכרחית לצורך שלהם להתרבות ולהפיץ. רבים מהפתוגנים העיקריים הנפוצים ביותר של בני אדם מדביקים רק בני אדם, אולם מחלות קשות רבות נגרמות על ידי אורגניזמים הנרכשים מהסביבה או שמדביקים מארחים שאינם בני אדם.
פתוגנים אופורטוניסטיים
פתוגנים אופורטוניסטיים עלולים לגרום למחלה זיהומית אצל מארח עם עמידות מדוכאת (מחסור בחיסון ) או אם יש להם גישה יוצאת דופן לחלק הפנימי של הגוף (למשל דרך טְרַאוּמָה ). זיהום אופורטוניסטי עלול להיגרם על ידי חיידקים שבדרך כלל נמצאים במגע עם המארח, כגון חיידקים פתוגניים או פטריות ב מערכת העיכול או ה דרכי הנשימה העליונות, והם עשויים לנבוע גם מחיידקים (שאינם מזיקים אחרת) שנרכשו ממארחים אחרים (כמו ב- Clostridium difficile קוליטיס ) או מהסביבה כתוצאה מ טְרַאוּמָטִי הקדמה (כמו ב כִּירוּרגִי זיהומים בפצעים או שברים מורכבים ). מחלה אופורטוניסטית מחייבת פגיעה בהגנות המארח, העלולות להתרחש כתוצאה מ פגמים גנטיים (כמו מחלה גרנולומטית כרונית ), חשיפה ל מיקרוביאלית סמים או מדכא חיסוני כימיקלים (כפי שעלול להתרחש בעקבות הַרעָלָה אוֹ מחלת הסרטן כימותרפיה ), חשיפה ל קרינה מייננת, או כתוצאה ממחלה זיהומית עם פעילות חיסונית (כמו עם חַצֶבֶת, מָלַרִיָה אוֹ מחלת HIV ). פתוגנים ראשוניים עלולים לגרום גם למחלה קשה יותר אצל מארח עם עמידות מדוכאת מאשר בדרך כלל במארח חסין.[17]
זיהום משני
בעוד שניתן לראות כמעט זיהום ראשוני כ- גורם שורש מהבעיה הבריאותית הנוכחית של הפרט, זיהום משני הוא המשך אוֹ תַסבִּיך של גורם שורש זה. לדוגמה, שחפת ריאתית הוא לעתים קרובות זיהום ראשוני, אך זיהום שקרה רק בגלל ש לשרוף אוֹ טראומה חודרת (גורם השורש) מותר גישה חריגה לרקמות עמוקות היא זיהום משני. פתוגנים ראשוניים לעיתים קרובות גורמים לזיהום ראשוני ולעיתים קרובות לגרום לזיהום משני. בדרך כלל, דלקות אופורטוניסטיות נתפסות כזיהומים משניים (בגלל מחסור בחיסון או פציעה היה הגורם הנטייה לנטייה).
סוגים אחרים של זיהום
סוגים אחרים של זיהום מורכבים מזיהום מעורב, iatrogenic, nosocomial, וקהילה. זיהום מעורב הוא זיהום הנגרם על ידי שני פתוגנים או יותר. דוגמה לכך היא דלקת התוספתן, הנגרמת על ידי Bacteroides fragilis ו- Escherichia coli. השנייה היא זיהום iatrogenic. סוג זה של זיהום הוא כזה המועבר מעובד רפואי לחולה. זיהום nosocomial הוא גם אחד המתרחש בסביבה בריאותית. זיהומים נוזוקומיאליים הם אלו הנרכשים במהלך שהות בבית חולים. לבסוף, זיהום שנרכש על ידי הקהילה הוא אחד בו הזיהום נרכש מקהילה שלמה.[15]
מדבק או לא
אחת הדרכים להוכיח כי מחלה נתונה מדבקת, היא לספק ההנחות של קוך (מוצע לראשונה על ידי רוברט קוך ), הדורשים כי ראשית, גורם זיהומיות ניתן לזהות רק בחולים הסובלים מהמחלה, ולא בביקורת בריאה, ושנית, כי חולים הסובלים מהגורם המדבק מפתחים גם הם את המחלה. הודעות אלה שימשו לראשונה בגילוי ש מיקובקטריה מינים גורמים שַׁחֶפֶת.
עם זאת, בדרך כלל לא ניתן לבדוק את ההנחות של קוך בפרקטיקה המודרנית מסיבות אתיות. הוכחתם תדרוש זיהום ניסיוני של אדם בריא עם מְחוֹלֵל מַחֲלָה מיוצר כתרבות טהורה. לעומת זאת, אפילו מחלות זיהומיות בעליל לא תמיד עומדות בקריטריונים המדבקים; לדוגמה, טרפונמה פלידום, הסיבתי ספירוצ'טה שֶׁל עַגֶבֶת, לא יכול להיות מְתוּרבָּת בַּמַבחֵנָה - אולם ניתן לטפח את האורגניזם בארנב אשכים. פחות ברור שתרבות טהורה מגיעה ממקור בעלי חיים המשמש כמארח מאשר כאשר היא נגזרת מחיידקים שמקורם בתרבית הצלחות.
אֶפִּידֶמִיוֹלוֹגִיָה, או המחקר והניתוח של מי, מדוע ואיפה מתרחשת מחלה ומה קובע אם אוכלוסיות שונות סובלות ממחלה, הוא כלי חשוב נוסף המשמש להבנת מחלות זיהומיות. אפידמיולוגים עשויים לקבוע הבדלים בין קבוצות באוכלוסייה, כגון האם קבוצות גיל מסוימות סובלות משיעור זיהום גדול יותר או פחות; האם קבוצות המתגוררות בשכונות שונות נוטות יותר להידבק; ועל ידי גורמים אחרים, כגון מין וגזע. החוקרים עשויים גם להעריך אם מחלה התפרצות הוא ספורדי, או סתם אירוע מזדמן; אֶנדֵמִי, עם רמה קבועה של מקרים קבועים המתרחשים באזור; מגפה, עם מספר מקרים שמתעוררים במהירות ובאופן בלתי רגיל באזור; אוֹ מגפה, שזו מגיפה עולמית. אם הגורם למחלה המדבקת אינו ידוע, ניתן להשתמש באפידמיולוגיה בכדי לסייע במעקב אחר מקורות הזיהום.
מדבקות
מחלות זיהומיות נקראות לעיתים מחלות מדבקות כאשר הם מועברים בקלות על ידי מגע עם אדם חולה או הפרשותיהם (למשל, שַׁפַעַת ). לפיכך, מחלה מדבקת היא תת קבוצה של מחלה זיהומית המועברת במיוחד או מועברת בקלות. סוגים אחרים של מחלות זיהומיות, העברות או תחלואה עם דרכי זיהום מיוחדות יותר, כגון העברה וקטורית או העברה מינית, בדרך כלל אינם נחשבים "מדבקים" ולעתים קרובות אינם דורשים בידוד רפואי (לפעמים נקרא באופן רופף בידוד ) של קורבנות. עם זאת, לא תמיד מכבדים קונוטציה מיוחדת זו של המילה "מדבק" ו"מחלה מדבקת "(העברות קלות) בשימוש פופולרי. מחלות זיהומיות מועברות בדרך כלל מאדם לאדם באמצעות מגע ישיר. סוגי המגע הם בין אדם לאדם והתפשטות טיפות. מגע עקיף כגון העברה מוטסית, חפצים מזוהמים, מזון ושתיית מים, מגע עם אדם מן החי, מאגרי בעלי חיים, עקיצות חרקים ומאגרי סביבה הם דרך נוספת להעברת מחלות זיהומיות.[18]
לפי מיקום אנטומי
ניתן לסווג זיהומים לפי המיקום האנטומי או מערכת אורגנית נגוע, כולל:
- דלקת בדרכי שתן
- זיהום בעור
- דלקת בדרכי הנשימה
- זיהום אודונטוגני (זיהום שמקורו בתוך שן או ברקמות הסמוכות)
- זיהומים בנרתיק
- זיהום תוך מי שפיר
בנוסף, מיקומים של דַלֶקֶת כאשר הזיהום הוא הגורם השכיח ביותר כולל דלקת ריאות, דַלֶקֶת קְרוֹם הַמוֹחַ ו סלפיטיטיס.
סימנים וסימפטומים
הסימפטומים של זיהום תלויים בסוג המחלה. סימנים מסוימים לזיהום משפיעים על כל הגוף באופן כללי, כגון עייפות, אובדן תיאבון, ירידה במשקל, חום, הזעות לילה, צמרמורות, כאבים וכאבים. אחרים ספציפיים לחלקי גוף בודדים, כגון עור פריחות, שיעול, או א נזלת.
במקרים מסוימים, מחלות זיהומיות עשויות להיות אסימפטומטי במשך הרבה או אפילו את כל מהלכיהם במארח נתון. במקרה האחרון, ניתן להגדיר את המחלה רק כ"מחלה "(שמשמעותה בהגדרה היא מחלה) אצל מארחים שחולים משנית לאחר מגע עם נשא ללא תסמינים. זיהום אינו שם נרדף למחלה זיהומית, מכיוון שחלק מהזיהומים אינם גורמים למחלה אצל מארח.[17]
בקטריאלי או ויראלי
מכיוון שזיהומים חיידקיים וויראליים עלולים לגרום לאותם סוגים של תסמינים, זה יכול להיות קשה להבחין מהו הגורם לזיהום ספציפי.[19] ההבדל בין השניים הוא חשוב, מכיוון שלא ניתן לרפא זיהומים נגיפיים אַנְטִיבִּיוֹטִיקָה ואילו זיהומים חיידקיים יכולים.[20]
| מאפיין | זיהום ויראלי | זיהום חיידקי |
|---|---|---|
| תסמינים אופייניים | באופן כללי, זיהומים נגיפיים הם מערכתיים. משמעות הדבר היא שהם מערבים חלקים רבים ושונים בגוף או יותר ממערכת גוף אחת בו זמנית; כלומר נזלת, גודש בסינוסים, שיעול, כאבי גוף וכו 'הם יכולים להיות מקומיים לפעמים כמו בוויראלי דַלֶקֶת הַלַחמִית או "עין ורודה" והרפס. רק כמה זיהומים נגיפיים כואבים, כמו הרפס. הכאב של זיהומים נגיפיים מתואר לעתים קרובות כגירוד או צריבה.[19] | הסימפטומים הקלאסיים של זיהום חיידקי הם אדמומיות מקומית, חום, נפיחות וכאב. אחד מסימני ההיכר של זיהום חיידקי הוא כאב מקומי, כאב שנמצא בחלק מסוים של הגוף. לדוגמא, אם חיתוך מתרחש ונדבק בחיידקים, כאב מתרחש במקום הזיהום. כאבי גרון חיידקיים מאופיינים לעיתים קרובות בכאבים רבים יותר בצד אחד של הגרון. An זיהום באוזן נוטה יותר להיות מאובחן כחיידקי אם הכאב מופיע באוזן אחת בלבד.[19] חתך המייצר מוגלה ונוזל בצבע חלבי הוא ככל הנראה נגוע.[יש צורך בבירור ][21] |
| גורם | נגיפים פתוגניים | חיידקים פתוגניים |
פתופיזיולוגיה
יש שרשרת אירועים כללית המתייחסת לזיהומים.[22] השתלשלות האירועים כוללת מספר שלבים - הכוללים את הגורם המדבק, המאגר, כניסה למארח רגיש, יציאה והעברה למארחים חדשים. כל אחד מהקישורים חייב להיות נוכח בסדר כרונולוגי כדי שהתפתחות זיהום תתפתח. הבנת צעדים אלה מסייעת לעובדי שירותי הבריאות למקד את הזיהום ולמנוע את התרחשותו מלכתחילה.[23]
קולוניזציה

זיהום מתחיל כאשר אורגניזם נכנס בהצלחה לגוף, גדל ומתרבה. זה מכונה קולוניזציה. רוב בני האדם אינם נגועים בקלות. לבעלי מערכת חיסונית נפגעת או מוחלשת יש רגישות מוגברת לזיהומים כרוניים או מתמשכים. אנשים שיש להם דיכוי מערכת החיסון רגישים במיוחד ל זיהומים אופורטוניסטיים. כניסה למארח בשעה ממשק פתוגן מארח, מתרחש בדרך כלל דרך רִירִית בפתחים כמו חלל פה, אף, עיניים, איברי המין, פי הטבעת או החיידק יכולים להיכנס דרך פצעים פתוחים. בעוד כמה אורגניזמים יכולים לצמוח באתר הכניסה הראשוני, רבים נודדים וגורמים לזיהום מערכתי באיברים שונים. ישנם פתוגנים שצומחים בתוך תאי המארח (תוך תאיים) ואילו אחרים גדלים באופן חופשי בנוזלי גוף.
פֶּצַע קולוניזציה מתייחסת למיקרואורגניזמים שאינם משכפלים בתוך הפצע, בעוד שבפצעים נגועים קיימים אורגניזמים משכפלים ורקמות נפגעות.[24] את כל אורגניזמים רב תאיים הם מושבתים במידה מסוימת על ידי אורגניזמים חיצוניים, והרוב המכריע של אלה קיים באחת הדדיות אוֹ קומנסל מערכת יחסים עם המארח. דוגמה לשעבר היא ה- חיידקים אנאירוביים מינים, המיישבים את ה יונק המעי הגס, ודוגמה של האחרונים הם המינים השונים של סטפילוקוקוס שקיימים ב עור אנושי. אף אחת מהקולוניזציות הללו אינה נחשבת לזיהום. ההבדל בין זיהום לקולוניזציה הוא לעתים קרובות רק עניין של נסיבות. אורגניזמים שאינם פתוגניים יכולים להפוך לפתוגניים בהתחשב בתנאים ספציפיים, ואפילו ביותר אַרסִי אורגניזם דורש נסיבות מסוימות כדי לגרום לזיהום מתפשר. חלק מהחיידקים המתיישבים, כגון Corynebacteria sp. ו סטרפטוקוקים של וירידנים, למנוע הידבקות והתיישבות של חיידקים פתוגניים ובכך לקיים קשר סימביוטי עם המארח, ומונע זיהום וזירוז מהיר ריפוי פצע.
המשתנים המעורבים בתוצאה של המארח שמתחסן על ידי פתוגן והתוצאה הסופית כוללים:
- מסלול הכניסה של מְחוֹלֵל מַחֲלָה והגישה לאזורים המארחים שהוא מקבל
- הפנימי אַרסִיוּת של האורגניזם המסוים
- הכמות או העומס של החיסון הראשוני
- ה חֲסִין מעמד המארח המושבת
כדוגמה, כמה סטפילוקוקל מינים נותרים מזיקים על העור, אך כאשר הם נמצאים בדרך כלל סטֵרִילִי שטח, כמו בקפסולה של א משותף או ה צֶפֶק, להכפיל ללא התנגדות ולגרום נזק.
עובדה מעניינת ש כרומטוגרפיה של גז - ספקטרומטריית מסה, 16S ריבוזומלי 16S אָנָלִיזָה, אומיקים, וטכנולוגיות מתקדמות אחרות הבהירו יותר לבני האדם בעשורים האחרונים היא שהתיישבות מיקרוביאלית נפוצה מאוד גם בסביבות שבני אדם חושבים עליהן כמעט סטֵרִילִי. מכיוון שזה נורמלי שיש קולוניזציה של חיידקים, קשה לדעת אילו פצעים כרוניים ניתן לסווג כנגועים וכמה סיכון להתקדם. למרות המספר העצום של פצעים שנצפו בפרקטיקה הקלינית, ישנם נתונים איכותיים מוגבלים לגבי סימפטומים וסימנים שהוערכו. סקירה של פצעים כרוניים בכתב העת "איגוד הבדיקות הקליניות הרציונליות של האגודה הרפואית האמריקאית" כימת את החשיבות של כאב מוגבר כאינדיקטור לזיהום.[28] הסקירה הראתה כי הממצא היעיל ביותר הוא עלייה ברמת הכאב [יחס הסבירות (LR), 11–20] הופכת את ההדבקה להרבה יותר סבירה, אך היעדר הכאב (טווח יחס הסבירות השלילי, 0.64–0.88) כן לא שוללים זיהום (סיכום LR 0.64–0.88).
מַחֲלָה
מַחֲלָה יכול להיווצר אם מנגנוני החיסון המגנים של המארח נפגעים והאורגניזם גורם נזק למארח. מיקרואורגניזמים עלול לגרום נזק לרקמות על ידי שחרור מגוון רעלים או אנזימים הרסניים. לדוגמה, קלוסטרידיום טטני משחרר רעלן המשתק את השרירים, ו סטפילוקוקוס משחרר רעלים המייצרים הלם ואלח דם. לא כל הגורמים המדבקים גורמים למחלות בכל המארחים. לדוגמא, פחות מ -5% מהאנשים הנגועים ב פּוֹלִיוֹ לפתח מחלה.[29] מצד שני, כמה גורמים זיהומיים הם מאוד ארסיים. ה פריון גורם מחלת הפרה המשוגעת ו מחלת קרויצפלד-יעקב תמיד הורג את כל בעלי החיים והאנשים הנגועים.
זיהומים מתמשכים מתרחשים מכיוון שהגוף אינו מסוגל לנקות את האורגניזם לאחר ההדבקה הראשונית. זיהומים מתמשכים מאופיינים בנוכחות מתמדת של האורגניזם המדבק, לעיתים קרובות כידבק סמוי עם הישנות חוזרת ונשנית של זיהום פעיל. ישנם וירוסים שיכולים לשמור על זיהום מתמשך על ידי הדבקת תאי גוף שונים. כמה נגיפים שנרכשו פעם לא עוזבים את הגוף. דוגמה טיפוסית היא נגיף הרפס, הנוטה להסתתר בעצבים ולהופעל מחדש כאשר מתרחשות נסיבות ספציפיות.
זיהומים מתמשכים גורמים למיליוני מקרי מוות ברחבי העולם מדי שנה.[30] זיהומים כרוניים על ידי טפילים מהווים תחלואה ותמותה גבוהה במדינות לא מפותחות רבות.
הפצה

כדי שמדביקים אורגניזמים לשרוד ולחזור על מחזור ההדבקה אצל מארחים אחרים, עליהם (או על צאצאיהם) לעזוב מאגר קיים ולגרום לזיהום במקום אחר. העברת זיהום יכולה להתרחש במסלולים פוטנציאליים רבים:
- קשר טיפות, הידוע גם בשם מסלול נשימה, ואת הזיהום שהתקבל ניתן לכנות מחלה מוטסת. אם אדם נגוע משתעל או מתעטש על אדם אחר המיקרואורגניזמים, המושבעים בטיפות חמות ולחות, עלולים לחדור לגוף דרך האף, הפה או משטחי העין.
- העברה בצואה-פה, שבהם מזונות או מים מזוהמים (על ידי אנשים שלא שוטפים ידיים לפני הכנת אוכל, או שביוב לא מטופל משוחרר לאספקת מי שתייה) והאנשים שאוכלים ושותים אותם נדבקים. פתוגנים נפוצים המועברים בצואה-דרך הפה כוללים ויבריו כולרה, ג'יארדיה מִין, וירוסים, אנטמבה היסטוליטיקה, אי קולי, ו תולעי קלטת.[31] מרבית הפתוגנים הללו גורמים גסטרואנטריטיס.
- העברה מינית, כאשר המחלה שנוצרה נקראת מחלה מועברת במגע המיני
- העברה דרך הפה, מחלות המועברות בעיקר באמצעים בעל פה עלולות להידבק במגע ישיר בעל פה כגון נשיקות, או על ידי מגע עקיף כגון על ידי שיתוף כוס שתייה או סיגריה.
- שידור במגע ישיר, חלק מהמחלות המועברות במגע ישיר כוללות רגל של ספורטאי, סַעֶפֶת ו יבלות
- העברת רכב, העברה דרך מאגר דומם (מזון, מים, אדמה).[32]
- שידור אנכי, ישירות מהאם ל- עוּבָּר, עוּבָּר או תינוק במהלך הֵרָיוֹן אוֹ לֵדָה. זה יכול להתרחש כתוצאה של זיהום קיים מראש או כזה שנרכש במהלך ההריון.
- Iatrogenic הפצה, עקב הליכים רפואיים כגון זריקה אוֹ הַשׁתָלָה של חומר נגוע.
- שידור וקטורי, מועבר על ידי א וֶקטוֹר, שהוא אורגניזם זה לא גורם מַחֲלָה את עצמו אבל זה משדר זיהום על ידי העברה פתוגנים מאחד מנחה לאחר.[33]
מערכת היחסים בין ארסיות לעומת העברות מורכב; אם מחלה קטלנית במהירות, המארח עלול למות לפני שניתן להעביר את החיידק למארח אחר.
אִבחוּן
הסעיף הזה צריך ציטוטים נוספים עבור אימות. (דצמבר 2019) (למד כיצד ומתי להסיר הודעת תבנית זו) |
אבחון של מחלות זיהומיות כרוך לפעמים בזיהוי גורם זיהומי במישרין או בעקיפין.[34] בפועל רוב המחלות הזיהומיות הקלות כמו יבלות, עורית מורסות, מערכת נשימה זיהומים ו מחלות שלשול מאובחנים על ידי המצגת הקלינית שלהם ומטופלים ללא ידיעה על הגורם הסיבתי הספציפי. המסקנות לגבי סיבת המחלה מבוססות על הסבירות שמטופל בא במגע עם גורם מסוים, נוכחות של חיידק בקהילה ושיקולים אפידמיולוגיים אחרים. בהינתן מאמץ מספיק, ניתן לזהות באופן ספציפי את כל גורמי הזיהום הידועים. עם זאת, יתרונות הזיהוי בדרך כלל עולים על העלות, מכיוון שלעתים קרובות אין טיפול ספציפי, הסיבה ברורה או התוצאה של זיהום היא שָׁפִיר.
אבחון של מחלות זיהומיות הוא כמעט תמיד ביוזמת היסטוריה רפואית ובדיקה גופנית. טכניקות זיהוי מפורטות יותר כוללות את התרבותם של גורמים זיהומיים המבודדים ממטופל. תרבות מאפשרת זיהוי של אורגניזמים זיהומיים על ידי בחינת תכונותיהם המיקרוסקופיות, על ידי גילוי נוכחות של חומרים המיוצרים על ידי פתוגנים ועל ידי זיהוי ישיר של אורגניזם על ידי הגנוטיפ שלו. טכניקות אחרות (כגון צילומי רנטגן, סריקות CAT, סריקות PET אוֹ NMR ) משמשים להפקת תמונות של חריגות פנימיות הנובעות מגידול של גורם זיהומי. התמונות שימושיות בזיהוי של עצם, למשל מוּרְסָה או א אנצפלופתיה ספוגיפורמית מיוצר על ידי א פריון.
אבחון סימפטומטי
האבחנה נעזרת בתסמינים המופיעים אצל כל אדם הסובל ממחלה מדבקת, אך בדרך כלל הוא זקוק לטכניקות אבחון נוספות בכדי לאשר את החשד. ישנם סימנים האופייניים במיוחד ומעידים על מחלה והם נקראים פתוגנומוני שלטים; אך אלה נדירים. לא כל הזיהומים הם סימפטומטיים.[35]
אצל ילדים הנוכחות של כִּחָלוֹן, נשימה מהירה, זלוף היקפי לקוי, או א פריחה פטרונית מגביר את הסיכון לזיהום חמור פי פי 5.[36] מדדים חשובים אחרים כוללים דאגה של ההורים, אינסטינקט קליני וטמפרטורה הגבוהה מ- 40 מעלות צלזיוס.[36]
תרבות מיקרוביאלית
תרבות מיקרוביולוגית הוא כלי עיקרי המשמש לאבחון מחלות זיהומיות. בתרבות מיקרוביאלית, א מדיום צמיחה מסופק עבור סוכן ספציפי. לאחר מכן נבדק דגימה שנלקחה מרקמה או נוזל שעלולים להיות חולים, בנוכחות נוכחות של גורם זיהומי המסוגל לצמוח בתוך המדיום. מרבית החיידקים הפתוגניים מגדלים בקלות על חומרים מזינים אגר, צורה של מדיום מוצק המספק פחמימות וחלבונים הדרושים לצמיחה של חיידק, יחד עם כמויות גדושות של מים. חיידק יחיד יצמח לתל גלוי על פני הצלחת הנקרא a מוֹשָׁבָה, שעשוי להיות מופרד ממושבות אחרות או להתמזג יחד ל"דשא ". הגודל, הצבע, הצורה והצורה של מושבה אופייניים למין החיידק, למערך הגנטי הספציפי שלה (שלו) מתח ), והסביבה התומכת בצמיחתה. מרכיבים אחרים מתווספים לעיתים קרובות לצלחת כדי לסייע בזיהוי. לוחות עשויים להכיל חומרים המאפשרים צמיחה של חיידקים מסוימים ולא של אחרים, או שמשנים את צבעם כתגובה לחיידקים מסוימים ולא לאחרים. פלטות בקטריולוגיות כמו אלה משמשות בדרך כלל בזיהוי קליני של חיידק מדבק. ניתן להשתמש בתרבית מיקרוביאלית לזיהוי וירוסים: המדיום, במקרה זה, להיות תאים שגדלו בתרבית שהנגיף יכול להדביק ואז לשנות או להרוג. במקרה של זיהוי נגיפי, אזור של תאים מתים נובע מגידול נגיפי, ומכונה "פלאק". אוקריוטי טפילים עשוי לגדל גם בתרבות כאמצעי לזיהוי גורם מסוים.
בהיעדר טכניקות תרבות צלחות מתאימות, ישנם חיידקים הדורשים תרבית בתוך בעלי חיים חיים. חיידקים כגון Mycobacterium leprae ו טרפונמה פלידום ניתן לגדל בבעלי חיים, אם כי טכניקות סרולוגיות ומיקרוסקופיות הופכות את השימוש בבעלי חיים מיותרים. נגיפים מזוהים בדרך כלל באמצעות חלופות לצמיחה בתרבית או בבעלי חיים. ייתכן וירוסים מסוימים גדלו עוברים ביצים. שיטת זיהוי שימושית נוספת היא קסנודיאגנוזה, או שימוש בווקטור לתמיכה בצמיחה של גורם זיהומי. מחלת שאגאס היא הדוגמה המשמעותית ביותר מכיוון שקשה להדגים באופן ישיר את נוכחותו של הגורם הסיבתי, טריפנוסומה קרוזי בחולה, ולכן מקשה על אבחנה סופית. במקרה זה, קסנודיאגנוזה כוללת שימוש ב- וֶקטוֹר של סוכן צ'אגאס טי קרוזי, לא נגוע טריאטום באג, שלוקח ארוחת דם מאדם החשוד כי נדבק. מאוחר יותר נבדק הבאג לצמיחה של טי קרוזי בתוך המעיים שלו.
מיקרוסקופיה
כלי עיקרי נוסף באבחון מחלות זיהומיות הוא מיקרוסקופיה. כמעט כל טכניקות התרבות שנדונו לעיל נשענות, בשלב מסוים, על בדיקה מיקרוסקופית לצורך זיהוי סופי של הגורם המדבק. מיקרוסקופיה יכולה להתבצע עם מכשירים פשוטים, כגון התרכובת מיקרוסקופ אור, או עם מכשירים מורכבים כמו מיקרוסקופ אלקטרונים. ניתן לראות דוגמאות המתקבלות ממטופלים ישירות במיקרוסקופ האור ולעתים קרובות יכולות לגרום לזיהוי במהירות. מיקרוסקופיה משמשת לעתים קרובות גם יחד עם ביוכימי הַכתָמָה טכניקות, וניתן להפוך אותן לספציפיות להפליא כאשר משתמשים בה בשילוב עם נוֹגְדָן טכניקות מבוססות. לדוגמא, השימוש ב נוגדנים נעשה באופן מלאכותי פלואורסצנטי (נוגדנים שכותרתו פלואורסצנטית) יכולים להיות מכוונים להיקשר ולזהות ספציפי אנטיגנים נוכח על פתוגן. א מיקרוסקופ פלואורסצנטי משמש אז לאיתור נוגדנים שכותרתו פלואורסצנטית הקשורים לאנטיגנים מופנמים בתוך דגימות קליניות או תאים מתורבתים. טכניקה זו שימושית במיוחד באבחון מחלות נגיפיות, כאשר מיקרוסקופ האור אינו מסוגל לזהות וירוס באופן ישיר.
פרוצדורות מיקרוסקופיות אחרות עשויות גם לסייע בזיהוי גורמים זיהומיים. כמעט כל התאים מוכתמים בקלות עם מספר בסיסים צבעים בשל אלקטרוסטטי משיכה בין מולקולות תאיות בעלות מטען שלילי לבין המטען החיובי על הצבע. תא הוא בדרך כלל שקוף תחת מיקרוסקופ, ושימוש בכתם מגביר את הניגודיות של התא עם הרקע שלו. מכתים תא עם צבע כגון ג'ימסה כתם או סגול קריסטל מאפשר למיקרוסקופ לתאר את גודלו, צורתו, מרכיביו הפנימיים והחיצוניים ואת קשריו לתאים אחרים. התגובה של חיידקים להליכי צביעה שונים משמשת ב סיווג טקסונומי גם של חיידקים. שתי שיטות, ה צביעת גראם וה חומצי מהיר כתם, הן הגישות הסטנדרטיות המשמשות לסיווג חיידקים ולאבחון מחלות. כתם הגראם מזהה את קבוצות החיידקים מיישמים ו אקטינובקטריה, שניהם מכילים הרבה פתוגנים אנושיים משמעותיים. הליך הצביעה המהיר בחומצה מזהה את הסוג האקטינובקטריאלי מיקובקטריום ו נוקארדיה.
בדיקות ביוכימיות
בדיקות ביוכימיות המשמשות לזיהוי גורמי זיהום כוללות איתור מטבולית אוֹ אנזימטית מוצרים האופייניים לחומר זיהומי מסוים. מאז חיידקים מתסיסים פחמימות בדפוסים האופייניים להם סוּג ו מִין, איתור תְסִיסָה מוצרים נפוצים בזיהוי חיידקים. חומצות, אלכוהול ו גזים בדרך כלל מתגלים בבדיקות אלה כאשר מגדלים חיידקים סֶלֶקטִיבִי מדיה נוזלית או מוצקה.
הבידוד של אנזימים מרקמה נגועה יכולה גם לספק בסיס לאבחון ביוכימי של מחלה זיהומית. לדוגמא, בני אדם אינם יכולים ליצור אף אחד מהם שכפול RNA ולא תעתיק הפוך ונוכחותם של אנזימים אלו אופיינית לסוגים ספציפיים של זיהומים נגיפיים. היכולת של החלבון הוויראלי המגלוטינין לאגד תאי דם אדומים יחד למטריצה הניתנת לזיהוי עשויה להיות מאופיינת כמבחן ביוכימי לזיהום נגיפי, אם כי באופן הדוק ההמגלוטינין אינו מהווה אֶנזִים ואין לו שום פונקציה מטבולית.
סרולוגית השיטות הן בדיקות רגישות ביותר, ספציפיות ולעיתים קרובות מהירות במיוחד המשמשות לזיהוי מיקרואורגניזמים. בדיקות אלה מבוססות על יכולתו של נוגדן להיקשר באופן ספציפי לאנטיגן. האנטיגן, בדרך כלל חלבון או פחמימה המיוצרים על ידי גורם זיהומי, נקשר על ידי הנוגדן. כריכה זו יוצרת שרשרת אירועים שיכולה להיות ברורה לעין בדרכים שונות, תלוי במבחן. לדוגמה, "דלקת גרון "מאובחן לעתים קרובות תוך מספר דקות, ומבוסס על הופעת אנטיגנים שיוצר הגורם הסיבתי, S. pyogenes, שנשלף מגרונו של המטופל בעזרת צמר גפן. בדיקות סרולוגיות, אם הן זמינות, הן בדרך כלל דרך הזיהוי המועדפת, אולם הבדיקות יקרות לפיתוח והריאגנטים המשמשים בבדיקה דורשים לעיתים קרובות קֵרוּר. כמה שיטות סרולוגיות הן יקרות ביותר, אם כי כאשר משתמשים בהן בדרך כלל, כמו למשל עם "בדיקת הסטרפט", הן יכולות להיות זולות.[17]
טכניקות סרולוגיות מורכבות פותחו למה שמכונה מבחני חיסון. מבחני חיסון יכולים להשתמש בנוגדן הבסיסי - קשירת אנטיגן כבסיס להפקת אות קרינת אלקטרו-מגנטי או חלקיקים, שניתן לזהות אותו באמצעות מכשור כלשהו. ניתן להשוות אות של אלמונים לזה של תקנים המאפשרים כימות של אנטיגן היעד. כדי לסייע באבחון של מחלות זיהומיות, מבחני חיסון יכולים לזהות או למדוד אנטיגנים מחומרים זיהומיים או מחלבונים שנוצרים על ידי אורגניזם נגוע בתגובה לסוכן זר. לדוגמא, ניתוח חיסוני A עשוי לזהות נוכחות של חלבון עילי מחלקיק הנגיף. לעומת זאת, חיסון ב 'עשוי לזהות או למדוד נוגדנים המיוצרים על ידי מערכת החיסון של האורגניזם שנועדו לנטרל ולאפשר את הרס הנגיף.
ניתן להשתמש במכשור לקריאת אותות קטנים במיוחד שנוצרו על ידי תגובות משניות המקושרות לקשירת הנוגדן - אנטיגן. המכשור יכול לשלוט על דגימה, שימוש בריאגנט, זמני תגובה, איתור אותות, חישוב תוצאות וניהול נתונים כדי להניב תהליך אוטומטי וחסכוני לאבחון מחלות זיהומיות.
אבחון מבוסס PCR
טכנולוגיות המבוססות על תגובת שרשרת פולימראז (PCR) שיטה תהפוך לסטנדרטים של זהב כמעט אבחון של העתיד הקרוב, מכמה סיבות. ראשית, קטלוג הגורמים המדבקים גדל עד כדי כך שזוהו כמעט כל הגורמים המדביקים המשמעותיים באוכלוסיית האדם. שנית, גורם זיהומי חייב לצמוח בגוף האדם כדי לגרום למחלות; בעצם עליו להגביר חומצות גרעין משלו בכדי לגרום למחלה. הגברה זו של חומצת גרעין ברקמות נגועות מציעה הזדמנות לאתר את הגורם המדבק באמצעות PCR. שלישית, הכלים החיוניים להפניית PCR, פריימרים, נגזרים מה- גנום של גורמים זיהומיים, ועם הזמן הגנומים האלה יהיו ידועים, אם הם כבר לא.
לפיכך, היכולת הטכנולוגית לאתר כל גורם מדבק במהירות ובאופן ספציפי קיימת כיום. החסימות היחידות שנותרו לשימוש ב- PCR ככלי אבחון סטנדרטי הן בעלותו וביישומו, שאף אחת מהן אינה ניתנת להתגברות. אבחנה של כמה מחלות לא תועיל לפיתוח שיטות PCR, כגון חלק מהמחלות clostridial מחלות (טֶטָנוּס ו בּוּטוּלִיזְם ). מחלות אלה הינן הרעלות ביולוגיות ביסודן על ידי מספר קטן יחסית של חיידקים מדבקים המייצרים עוצמה רבה נוירוטוקסינים. ריבוי משמעותי של החומר המדבק אינו מתרחש, זה מגביל את היכולת של PCR לזהות נוכחות של חיידקים כלשהם.
רצף מטאגנומי
בהתחשב במגוון הרחב של חיידקים, נגיפים ופתוגנים אחרים הגורמים למחלות מתישות ומסכנות חיים, היכולת לזהות במהירות את הגורם לזיהום חשובה אך לעיתים קרובות מאתגרת. לדוגמא, יותר ממחצית המקרים של דַלֶקֶת הַמוֹחַ, מחלה קשה הפוגעת במוח, נותרת ללא אבחנה, למרות בדיקות מקיפות בשיטות מעבדה קליניות משוכללות. מטאגנומיקה נחקר בימים אלה לשימוש קליני, ומראה הבטחה כדרך רגישה ומהירה לאבחון זיהום באמצעות בדיקה כוללת הכוללת. בדיקה זו דומה לבדיקות ה- PCR הנוכחיות; עם זאת, הגברה של החומר הגנטי אינה משוחדת ולא בשימוש פריימרים עבור גורם זיהומי ספציפי. צעד הגברה זה מלווה ברצף הדור הבא השוואות יישור באמצעות מאגרי מידע גדולים של אלפי גנומים אורגניזמים וויראליים.
רצף מטוגנומי יכול להוכיח שימושית במיוחד לאבחון כאשר המטופל נמצא חסרת חיסון. מגוון רחב יותר ויותר של חומרים זיהומיים עלול לגרום נזק חמור לאנשים הסובלים מדיכוי חיסוני, ולכן לרוב הסינון הקליני חייב להיות רחב יותר. בנוסף, ביטוי הסימפטומים לרוב אינו טיפוסי, מה שמקשה על האבחנה הקלינית על בסיס הצגה. שלישית, שיטות אבחון המסתמכות על איתור נוגדנים נוטות יותר להיכשל. לכן רצוי מאוד לבצע בדיקה רחבה ורגישה לפתוגנים המאתרת נוכחות של חומר זיהומי ולא נוגדנים.
אינדיקציה למבחנים
בדרך כלל יש סִימָן לזיהוי ספציפי של גורם מדבק רק כאשר זיהוי כזה יכול לסייע בטיפול או במניעת המחלה, או לקידום הידע על מהלך המחלה לפני פיתוח אמצעים טיפוליים או מונעים יעילים. לדוגמא, בתחילת שנות השמונים, לפני הופעתו של AZT לטיפול ב איידס, the course of the disease was closely followed by monitoring the composition of patient blood samples, even though the outcome would not offer the patient any further treatment options. In part, these studies on the appearance of HIV in specific communities permitted the advancement of השערות as to the route of transmission of the virus. By understanding how the disease was transmitted, resources could be targeted to the communities at greatest risk in campaigns aimed at reducing the number of new infections. המסוים serological diagnostic identification, and later genotypic or molecular identification, of HIV also enabled the development of hypotheses as to the זְמַנִי ו גיאוגרפי origins of the virus, as well as a myriad of other hypothesis.[17] The development of molecular diagnostic tools have enabled physicians and researchers to monitor the efficacy of treatment with תרופות אנטי-רטרו-ויראליות. Molecular diagnostics are now commonly used to identify HIV in healthy people long before the onset of illness and have been used to demonstrate the existence of people who are genetically resistant to HIV infection. Thus, while there still is no cure for AIDS, there is great therapeutic and predictive benefit to identifying the virus and monitoring the virus levels within the blood of infected individuals, both for the patient and for the community at large.
מְנִיעָה
Techniques like hand washing, wearing gowns, and wearing face masks can help prevent infections from being passed from one person to another. Aseptic technique was introduced in medicine and surgery in the late 19th century and greatly reduced the incidence of infections caused by surgery. תָכוּף שטיפת ידיים remains the most important defense against the spread of unwanted organisms.[38] There are other forms of prevention such as avoiding the use of illicit drugs, using a קוֹנדוֹם, wearing gloves, and having a healthy lifestyle with a balanced diet and regular exercise. Cooking foods well and avoiding foods that have been left outside for a long time is also important.
Antimicrobial substances used to prevent transmission of infections include:
- חיטוי, which are applied to living רִקמָה /עור
- חומרי חיטוי, אשר הורסים מיקרואורגניזמים המצויים על עצמים שאינם חיים.
- אַנְטִיבִּיוֹטִיקָה, שקוראים לו מוֹנֵעַ when given as prevention rather as treatment of infection. However, long term use of antibiotics leads to resistance of bacteria. While humans do not become immune to antibiotics, the bacteria does. Thus, avoiding using antibiotics longer than necessary helps preventing bacteria from forming mutations that aide in antibiotic resistance.
One of the ways to prevent or slow down the transmission of infectious diseases is to recognize the different characteristics of various diseases.[39] Some critical disease characteristics that should be evaluated include אַרסִיוּת, distance traveled by victims, and level of contagiousness. The human strains of אבולה virus, for example, incapacitate their victims extremely quickly and kill them soon after. As a result, the victims of this disease do not have the opportunity to travel very far from the initial infection zone.[40] Also, this virus must spread through skin lesions or permeable membranes such as the eye. Thus, the initial stage of אבולה is not very contagious since its victims experience only internal hemorrhaging. As a result of the above features, the spread of Ebola is very rapid and usually stays within a relatively confined geographical area. לעומת זאת, ה נגיף חסר אנושי (HIV ) kills its victims very slowly by attacking their immune system.[17] As a result, many of its victims transmit the virus to other individuals before even realizing that they are carrying the disease. Also, the relatively low virulence allows its victims to travel long distances, increasing the likelihood of an מגפה.
Another effective way to decrease the transmission rate of infectious diseases is to recognize the effects of רשתות עולם קטן.[39] In epidemics, there are often extensive interactions within hubs or groups of infected individuals and other interactions within discrete hubs of susceptible individuals. Despite the low interaction between discrete hubs, the disease can jump to and spread in a susceptible hub via a single or few interactions with an infected hub. Thus, infection rates in small-world networks can be reduced somewhat if interactions between individuals within infected hubs are eliminated (Figure 1). However, infection rates can be drastically reduced if the main focus is on the prevention of transmission jumps between hubs. The use of needle exchange programs in areas with a high density of drug users with HIV is an example of the successful implementation of this treatment method. [6][צורך בציטוט מלא ] Another example is the use of ring culling or vaccination of potentially susceptible livestock in adjacent farms to prevent the spread of the foot-and-mouth virus in 2001.[41]
A general method to prevent transmission of וֶקטוֹר -borne pathogens is הדברה.
In cases where infection is merely suspected, individuals may be בהסגר until the incubation period has passed and the disease manifests itself or the person remains healthy. Groups may undergo quarantine, or in the case of communities, a קורטון סאניטייר may be imposed to prevent infection from spreading beyond the community, or in the case of protective sequestration, into a community. Public health authorities may implement other forms of ריחוק חברתי, such as school closings, to control an epidemic.
חֲסִינוּת

Infection with most pathogens does not result in death of the host and the offending organism is ultimately cleared after the symptoms of the disease have waned.[16] תהליך זה דורש immune mechanisms to kill or inactivate the inoculum של הפתוגן. Specific acquired חֲסִינוּת against infectious diseases may be mediated by נוגדנים ו / או לימפוציטים T. Immunity mediated by these two factors may be manifested by:
- a direct effect upon a pathogen, such as antibody-initiated מַשׁלִים -dependent bacteriolysis, opsonoization, פגוציטוזיס and killing, as occurs for some bacteria,
- neutralization of viruses so that these organisms cannot enter cells,
- or by T lymphocytes, which will kill a cell parasitized by a microorganism.
The immune system response to a microorganism often causes symptoms such as a high חום ו דַלֶקֶת, and has the potential to be more devastating than direct damage caused by a microbe.[17]
Resistance to infection (חֲסִינוּת ) may be acquired following a disease, by asymptomatic carriage of the pathogen, by harboring an organism with a similar structure (crossreacting), or by חיסון. Knowledge of the protective antigens and specific acquired host immune factors is more complete for primary pathogens than for opportunistic pathogens.There is also the phenomenon of חסינות העדר which offers a measure of protection to those otherwise vulnerable people when a large enough proportion of the population has acquired immunity from certain infections.
Immune resistance to an infectious disease requires a critical level of either antigen-specific antibodies and/or T cells when the host encounters the pathogen. Some individuals develop natural נַסיוֹב antibodies to the surface פוליסכרידים of some agents although they have had little or no contact with the agent, these natural antibodies confer specific protection to adults and are passively transmitted to newborns.
מארחים גורמים גנטיים
The organism that is the target of an infecting action of a specific infectious agent is called the host. The host harbouring an agent that is in a mature or sexually active stage phase is called the definitive host. The intermediate host comes in contact during the larvae stage. A host can be anything living and can attain to asexual and sexual reproduction.[42]The clearance of the pathogens, either treatment-induced or spontaneous, it can be influenced by the genetic variants carried by the individual patients. For instance, for genotype 1 hepatitis C treated with Pegylated interferon-alpha-2a אוֹ Pegylated interferon-alpha-2b (brand names Pegasys or PEG-Intron) combined with ריבאווירין, it has been shown that genetic polymorphisms near the human IL28B gene, encoding interferon lambda 3, are associated with significant differences in the treatment-induced clearance of the virus. This finding, originally reported in Nature,[43] showed that genotype 1 hepatitis C patients carrying certain genetic variant alleles near the IL28B gene are more possibly to achieve sustained virological response after the treatment than others. Later report from Nature[44] demonstrated that the same genetic variants are also associated with the natural clearance of the genotype 1 hepatitis C virus.
טיפולים
When infection attacks the body, anti-infective drugs can suppress the infection. Several broad types of anti-infective drugs exist, depending on the type of organism targeted; they include antibacterial (אַנטִיבִּיוֹטִי; לְרַבּוֹת antitubercular ), אנטי-ויראלי, אנטי פטרייתי ו antiparasitic (לְרַבּוֹת אנטי פרוטוזואלית ו אנטי-הלמינטית ) agents. Depending on the severity and the type of infection, the antibiotic may be given by mouth or by injection, or may be applied באופן מקומי. Severe infections of the מוֹחַ are usually treated with תוֹך וְרִידִי אַנְטִיבִּיוֹטִיקָה. Sometimes, multiple antibiotics are used in case there is הִתנַגְדוּת to one antibiotic. Antibiotics only work for bacteria and do not affect viruses. Antibiotics work by slowing down the multiplication of bacteria or killing the bacteria. The most common classes of antibiotics used in medicine include פֵּנִיצִילִין, קפלוספורינים, אמינוגליקוזידים, מקרולידים, קווינולונים ו טטרציקלינים.[45][46]
Not all infections require treatment, and for many מגביל את עצמו infections the treatment may cause more side-effects than benefits. אחזקות אנטי מיקרוביאלית is the concept that healthcare providers should treat an infection with an antimicrobial that specifically works well for the target pathogen for the shortest amount of time and to only treat when there is a known or highly suspected pathogen that will respond to the medication.[47]
אֶפִּידֶמִיוֹלוֹגִיָה


In 2010, about 10 million people died of infectious diseases.[49]
ה ארגון הבריאות העולמי collects information on global deaths by International Classification of Disease (ICD) code categories. The following table lists the top infectious disease by number of deaths in 2002. 1993 data is included for comparison.
| דַרגָה | סיבת המוות | Deaths 2002 (במיליונים) | אחוז של all deaths | Deaths 1993 (במיליונים) | 1993 Rank |
|---|---|---|---|---|---|
| לא | All infectious diseases | 14.7 | 25.9% | 16.4 | 32.2% |
| 1 | זיהומים בדרכי הנשימה התחתונות[52] | 3.9 | 6.9% | 4.1 | 1 |
| 2 | HIV /איידס | 2.8 | 4.9% | 0.7 | 7 |
| 3 | מחלות שלשול[53] | 1.8 | 3.2% | 3.0 | 2 |
| 4 | שַׁחֶפֶת (שַׁחֶפֶת) | 1.6 | 2.7% | 2.7 | 3 |
| 5 | מָלַרִיָה | 1.3 | 2.2% | 2.0 | 4 |
| 6 | חַצֶבֶת | 0.6 | 1.1% | 1.1 | 5 |
| 7 | שעלת | 0.29 | 0.5% | 0.36 | 7 |
| 8 | טֶטָנוּס | 0.21 | 0.4% | 0.15 | 12 |
| 9 | דַלֶקֶת קְרוֹם הַמוֹחַ | 0.17 | 0.3% | 0.25 | 8 |
| 10 | עַגֶבֶת | 0.16 | 0.3% | 0.19 | 11 |
| 11 | הפטיטיס B | 0.10 | 0.2% | 0.93 | 6 |
| 12–17 | מחלות טרופיות (6)[54] | 0.13 | 0.2% | 0.53 | 9, 10, 16–18 |
| Note: Other causes of death include maternal and perinatal conditions (5.2%), nutritional deficiencies (0.9%), noncommunicable conditions (58.8%), and injuries (9.1%). | |||||
The top three single agent/disease killers are HIV /איידס, שַׁחֶפֶת ו מָלַרִיָה. While the number of deaths due to nearly every disease have decreased, deaths due to HIV/AIDS have increased fourfold. Childhood diseases include שעלת, פוליומיליטיס, דִיפטֶרִיָה, חַצֶבֶת ו טֶטָנוּס. Children also make up a large percentage of lower respiratory and diarrheal deaths. In 2012, approximately 3.1 million people have died due to lower respiratory infections, making it the number 4 leading cause of death in the world.[55]
Historic pandemics
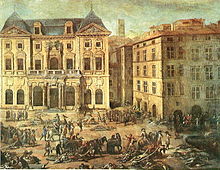
With their potential for unpredictable and explosive impacts, infectious diseases have been major actors in human הִיסטוֹרִיָה.[56] א מגפה (or global מגפה ) is a disease that affects people over an extensive geographical area. לדוגמה:
- מכת יוסטיניאנוס, from 541 to 542, killed between 50% and 60% of Europe's population.[57]
- ה מוות שחור of 1347 to 1352 killed 25 million in Europe over 5 years. The plague reduced the old world population from an estimated 450 million to between 350 and 375 million in the 14th century.
- ההקדמה של אֲבַעבּוּעוֹת, measles, and טִיפוּס to the areas of Central and South America by European explorers during the 15th and 16th centuries caused pandemics among the native inhabitants. Between 1518 and 1568 disease pandemics are said to have caused the population of מקסיקו to fall from 20 million to 3 million.[58]
- האירופאי הראשון שַׁפַעַת epidemic occurred between 1556 and 1560, with an estimated mortality rate of 20%.[58]
- אֲבַעבּוּעוֹת killed an estimated 60 million Europeans during the 18th century[59] (approximately 400,000 per year).[60] Up to 30% of those infected, including 80% of the children under 5 years of age, died from the disease, and one-third of the survivors went blind.[61]
- במאה ה 19, שַׁחֶפֶת killed an estimated one-quarter of the adult population of Europe;[62] by 1918 one in six deaths in France were still caused by TB.
- The Influenza Pandemic of 1918 (or the שפעת ספרדית ) killed 25–50 million people (about 2% of world population of 1.7 billion).[63] היום שַׁפַעַת kills about 250,000 to 500,000 worldwide each year.
Emerging diseases
In most cases, microorganisms live in harmony with their hosts via הֲדָדִי אוֹ קומנסל אינטראקציות. Diseases can emerge when existing parasites become pathogenic or when new pathogenic parasites enter a new host.
- התפתחות משותפת בֵּין טַפִּיל ו מנחה can lead to hosts becoming עָמִיד בִּפְנֵי to the parasites or the parasites may evolve greater אַרסִיוּת, מוביל ל immunopathological disease.
- Human activity is involved with many מחלות זיהומיות מתפתחות, כמו שינוי סביבתי enabling a parasite to occupy new נישות. When that happens, a מְחוֹלֵל מַחֲלָה that had been confined to a remote habitat has a wider distribution and possibly a new אורגניזם מארח. Parasites jumping from nonhuman to human hosts are known as zoonoses. Under disease invasion, when a parasite invades a new host species, it may become pathogenic in the new host.[64]
Several human activities have led to the emergence of זואונוטי human pathogens, including viruses, bacteria, protozoa, and rickettsia,[65] and spread of נושא וקטור diseases,[64] ראה גם globalization and disease ו מחלת חיות בר:
- Encroachment on wildlife בתי גידול. The construction of new villages and housing developments in rural areas force animals to live in dense populations, creating opportunities for microbes to mutate and emerge.[66]
- שינויים ב חַקלָאוּת. The introduction of new crops attracts new crop pests and the microbes they carry to farming communities, exposing people to unfamiliar diseases.
- ההרס של יערות גשם. As countries make use of their rain forests, by building roads through forests and clearing areas for settlement or commercial ventures, people encounter insects and other animals harboring previously unknown microorganisms.
- לא נשלט עִיוּר. The rapid growth of cities in many developing countries tends to concentrate large numbers of people into crowded areas with poor sanitation. These conditions foster transmission of contagious diseases.
- מוֹדֶרנִי תַחְבּוּרָה. Ships and other cargo carriers often harbor unintended "passengers", that can spread diseases to faraway destinations. While with international jet-airplane travel, people infected with a disease can carry it to distant lands, or home to their families, before their first symptoms appear.
תורת החיידקים

ב יָמֵי קֶדֶם, ה יווני הִיסטוֹרִיוֹן תוקידידס (c. 460 – c. 400 BCE) was the first person to write, in his account of the plague of Athens, that diseases could spread from an infected person to others.[67][68] בו On the Different Types of Fever (c. AD 175), the Greco-Roman physician גאלן speculated that plagues were spread by "certain seeds of plague", which were present in the air.[69] בתוך ה סושרותא סמחיטה, the ancient Indian physician Sushruta theorized: "Leprosy, fever, consumption, diseases of the eye, and other infectious diseases spread from one person to another by sexual union, physical contact, eating together, sleeping together, sitting together, and the use of same clothes, garlands and pastes."[70][71] This book has been dated to about the sixth century BC.[72]
A basic form of contagion theory was proposed by פַּרסִית רוֹפֵא אבן סינא (known as Avicenna in Europe) in קנון הרפואה (1025), which later became the most authoritative medical textbook in Europe up until the 16th century. In Book IV of the קָנוֹן, Ibn Sina discussed מגיפות, outlining the classical תורת המיסמה and attempting to blend it with his own early contagion theory. He mentioned that people can transmit disease to others by breath, noted contagion with שַׁחֶפֶת, and discussed the transmission of disease through water and dirt.[73] The concept of invisible contagion was later discussed by several חוקרי האיסלאם בתוך ה הסולטנות האיובית who referred to them as najasat ("impure substances"). ה fiqh מְלוּמָד אבן אל-חאג 'אל-עבדרי (c. 1250–1336), while discussing Islamic diet ו גֵהוּת, gave warnings about how contagion can contaminate water, food, and garments, and could spread through the water supply, and may have implied contagion to be unseen particles.[74]
כאשר מוות שחור מגפת דבר השיג אל-אנדלוס in the 14th century, the Arab physicians Ibn Khatima (c. 1369) and אבן אל-חטיב (1313–1374) hypothesised that infectious diseases were caused by "minute bodies" and described how they can be transmitted through garments, vessels and earrings.[75] Ideas of contagion became more popular in Europe during the רֵנֵסַנס, particularly through the writing of the Italian physician Girolamo Fracastoro.[76] Anton van Leeuwenhoek (1632–1723) advanced the science of מיקרוסקופיה by being the first to observe microorganisms, allowing for easy visualization of bacteria.
In the mid-19th century ג'ון סנואו ו ויליאם באד did important work demonstrating the contagiousness of typhoid and cholera through contaminated water. Both are credited with decreasing epidemics of cholera in their towns by implementing measures to prevent contamination of water.[77] לואיס פסטר proved beyond doubt that certain diseases are caused by infectious agents, and developed a vaccine for רבנים. רוברט קוך, provided the study of infectious diseases with a scientific basis known as Koch's postulates. אדוארד ג'נר, ג'ונאס סאלק ו אלברט סבין developed effective vaccines for אֲבַעבּוּעוֹת ו פּוֹלִיוֹ, which would later result in the עֲקִירָה and near-eradication of these diseases, respectively. אלכסנדר פלמינג discovered the world's first אַנטִיבִּיוֹטִי, פֵּנִיצִילִין, which Florey and Chain then developed. גרהרד דומאגק מפותח sulphonamides, the first broad spectrum מְלָאכוּתִי antibacterial drugs.
מומחים רפואיים
ה טיפול רפואי of infectious diseases falls into the תחום רפואי שֶׁל Infectious Disease and in some cases the study of propagation pertains to the field of אֶפִּידֶמִיוֹלוֹגִיָה. Generally, infections are initially diagnosed by טיפול ראשוני physicians or רפואה פנימית מומחים. For example, an "uncomplicated" דלקת ריאות will generally be treated by the רופא פנימי או ה רופא ריאות (lung physician). The work of the infectious diseases specialist therefore entails working with both patients and general practitioners, as well as laboratory scientists, immunologists, bacteriologists and other specialists.
An infectious disease team may be alerted when:
- The disease has not been definitively diagnosed after an initial workup
- The patient is חסרת חיסון (למשל ב איידס or after כימותרפיה );
- ה גורם זיהומיות is of an uncommon nature (e.g. מחלות טרופיות );
- The disease has not responded to first line אַנְטִיבִּיוֹטִיקָה;
- The disease might be dangerous to other patients, and the patient might have to be isolated
חברה ותרבות
A number of studies have reported associations between pathogen load in an area and human behavior. Higher pathogen load is associated with decreased size of ethnic and religious groups in an area. This may be due high pathogen load favoring avoidance of other groups, which may reduce pathogen transmission, or a high pathogen load preventing the creation of large settlements and armies that enforce a common culture. Higher pathogen load is also associated with more restricted sexual behavior, which may reduce pathogen transmission. It also associated with higher preferences for health and attractiveness in mates. גבוה יותר fertility rates and shorter or less parental care per child is another association that may be a compensation for the higher mortality rate. There is also an association with פוליגניה which may be due to higher pathogen load, making selecting males with a high genetic resistance increasingly important. Higher pathogen load is also associated with more collectivism and less individualism, which may limit contacts with outside groups and infections. There are alternative explanations for at least some of the associations although some of these explanations may in turn ultimately be due to pathogen load. Thus, polygyny may also be due to a lower male:female ratio in these areas but this may ultimately be due to male infants having increased mortality from infectious diseases. Another example is that poor socioeconomic factors may ultimately in part be due to high pathogen load preventing economic development.[78]
שיא מאובנים

Evidence of infection in fossil remains is a subject of interest for paleopathologists, scientists who study occurrences of injuries and illness in extinct life forms. Signs of infection have been discovered in the bones of carnivorous dinosaurs. When present, however, these infections seem to tend to be confined to only small regions of the body. A skull attributed to the early carnivorous dinosaur Herrerasaurus ischigualastensis exhibits pit-like wounds surrounded by swollen and porous bone. The unusual texture of the bone around the wounds suggests they were afflicted by a short-lived, non-lethal infection. Scientists who studied the skull speculated that the bite marks were received in a fight with another הררסאורוס. Other carnivorous dinosaurs with documented evidence of infection include אקרוקנטוזאורוס, אלוזאור, טירנוזאורוס and a tyrannosaur from the Kirtland Formation. The infections from both tyrannosaurs were received by being bitten during a fight, like the הררסאורוס דוּגמָה.[79]
חלל חיצון
ניסוי במעבורת החלל בשנת 2006 מצא זאת Salmonella typhimurium, a bacterium that can cause הרעלת מזון, הפך לארסי יותר כאשר טיפחו אותו בחלל.[80] ב- 29 באפריל 2013, מדענים במכון הפוליטכני של רנסלאייר, במימון נאס"א, דיווח כי במהלך טיסת חלל על תחנת חלל בינלאומית, חיידקים נראה כי הם מסתגלים ל סביבת חלל בדרכים "שלא נצפו על כדור הארץ" ובדרכים ש"יכולות להוביל לגידול בצמיחה ו אַרסִיוּת ".[81] לאחרונה, בשנת 2017, בַּקטֶרִיָה נמצאו עמידים יותר בפני אַנְטִיבִּיוֹטִיקָה ולשגשג בחוסר המשקל הקרוב של החלל.[82] מיקרואורגניזמים נצפו לשרוד את לִשְׁאוֹב של החלל החיצון.[83][84]
ראה גם
- מרכזי משאבים ביואינפורמטיקה for Infectious Diseases
- סכנה ביולוגית
- מחלה הנגרמת בדם
- זיהום משותף
- קונצנזוס קופנהגן
- Cordon sanitaire
- Disease diffusion mapping
- מעבר אפידמיולוגי
- מחלה הנישאת במזון
- טיפול גנטי
- היסטוריה של הרפואה
- זיהום שנרכש על ידי בית חולים
- מיגור מחלות זיהומיות
- פרויקט מיקרוביום אנושי
- בקרת זיהום
- בידוד (בריאות)
- רשימת חיידקי הנרתיק החיידקית
- רשימת גורמי המוות לפי שיעור
- רשימת מחלות הנגרמות על ידי חרקים
- רשימת מגיפות
- רשימת מחלות זיהומיות
- דוגמנות מתמטית של מחלות זיהומיות
- Membrane vesicle trafficking
- ריבוי זיהום
- מחלות טרופיות מוזנחות
- מעקב זקיף
- ריחוק חברתי
- מדגם אפידמיולוגי ספטיוטמפורלי (STEM)
- זיהום בשפך
- צפיפות מארח הסף
- העברה (רפואה)
- Ubi pus, ibi evacua (Latin: "where there is מוּגלָה, there evacuate it")
- מחלות הניתנות למניעת חיסון
- מחלות זיהומיות המועברות במים
הפניות
- ^ Definition of "infection" from several medical dictionaries – Retrieved on 2012-04-03
- ^ "Utilizing antibiotics agents effectively will preserve present day medication". News Ghana. 21 בנובמבר 2015. הוחזר 21 בנובמבר 2015.
- ^ "Types of Fungal Diseases". www.cdc.gov. 2019-06-27. הוחזר 2019-12-09.
- ^ Mada, Pradeep Kumar; Jamil, Radia T.; Alam, Mohammed U. (2019), "Cryptococcus (Cryptococcosis)", StatPearls, הוצאת StatPearls, PMID 28613714, אוחזר 2019-12-09
- ^ "About Parasites". www.cdc.gov. 2019-02-25. הוחזר 2019-12-09.
- ^ Brown, Peter J. (1987). "Microparasites and Macroparasites". אנתרופולוגיה תרבותית. 2 (1): 155–71. דוי:10.1525/can.1987.2.1.02a00120. JSTOR 656401.
- ^ Alberto Signore (2013). "About inflammation and infection" (PDF). מחקר EJNMMI. 8 (3).
- ^ GBD 2013 תמותה וגורמי מוות, משתפי פעולה (17 בדצמבר 2014). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study". אִזְמֵל. 385 (9963): 117–71. דוי:10.1016 / S0140-6736 (14) 61682-2. PMC 4340604. PMID 25530442.
- ^ "Infectious Disease, Internal Medicine". Association of American Medical Colleges. הועבר לארכיון מ המקורי בתאריך 06-02-2015. הוחזר 2015-08-20.
Infectious disease is the subspecialty of internal medicine dealing with the diagnosis and treatment of communicable diseases of all types, in all organs, and in all ages of patients.
- ^ Kayser, Fritz H; Kurt A Bienz; Johannes Eckert; Rolf M Zinkernagel (2005). מיקרוביולוגיה רפואית. שטוטגרט: גאורג תימה ורלאג. עמ ' 398. ISBN 978-3-13-131991-3.
- ^ Grinde, Bjørn (2013-10-25). "Herpesviruses: latency and reactivation – viral strategies and host response". כתב העת למיקרוביולוגיה אוראלית. 5: 22766. דוי:10.3402/jom.v5i0.22766. ISSN 0901-8328. PMC 3809354. PMID 24167660.
- ^ אלסבייה, מילון הרפואה המאויר של דורלנד, אלסבייה.
- ^ "Acute infections (MPKB)". mpkb.org. הוחזר 2019-12-09.
- ^ Boldogh, Istvan; Albrecht, Thomas; Porter, David D. (1996), Baron, Samuel (ed.), "Persistent Viral Infections", מיקרוביולוגיה רפואית (מהדורה רביעית), סניף הרפואה של אוניברסיטת טקסס בגלווסטון, ISBN 978-0-9631172-1-2, PMID 21413348, אוחזר 2020-01-23
- ^ א ב Foster, John (2018). מִיקרוֹבִּיוֹלוֹגִיָה. ניו יורק: נורטון. עמ ' 39. ISBN 978-0-393-60257-9.
- ^ א ב This section incorporates נחלת הכלל materials included in the text: מיקרוביולוגיה רפואית Fourth Edition: פרק 8 (1996). Baron, Samuel MD. סניף הרפואה של אוניברסיטת טקסס בגלווסטון. מיקרוביולוגיה רפואית. University of Texas Medical Branch at Galveston. 1996. ISBN 9780963117212. Archived from the original on June 29, 2009. הוחזר 2013-11-27.CS1 maint: BOT: לא ידוע על סטטוס ה- url המקורי (קישור)
- ^ א ב ג ד ה f ראיין KJ, ריי CG, עורכים. (2004). מיקרוביולוגיה רפואית של שריס (מהדורה רביעית). היל מקגרו. ISBN 978-0-8385-8529-0.
- ^ Higurea & Pietrangelo 2016[דף נדרש ]
- ^ א ב ג "Bacterial vs. Viral Infections – Do You Know the Difference?" National Information Program on Antibiotics
- ^ Robert N. Golden; Fred Peterson (2009). The Truth About Illness and Disease. הוצאת אינפובייס. עמ ' 181. ISBN 978-1438126371.
- ^ "הַדבָּקָה". Rencare. הועבר לארכיון מ המקורי ב -5 במרץ 2012. הוחזר 4 ביולי 2013.
- ^ מחזור זיהום – Retrieved on 2010-01-21 הועבר בארכיון May 17, 2014, at the מכונת Wayback
- ^ Understanding Infectious Diseases הועבר בארכיון 2009-09-24 ב מכונת Wayback Science.Education.Nih.Gov article – Retrieved on 2010-01-21
- ^ Negut, Irina; Grumezescu, Valentina; Grumezescu, Alexandru Mihai (2018-09-18). "Treatment Strategies for Infected Wounds". מולקולות. 23 (9): 2392. דוי:10.3390/molecules23092392. ISSN 1420-3049. PMC 6225154. PMID 30231567.
- ^ Duerkop, Breck A; Hooper, Lora V (2013-07-01). "Resident viruses and their interactions with the immune system". אימונולוגיה טבעית. 14 (7): 654–59. דוי:10.1038/ni.2614. PMC 3760236. PMID 23778792.
- ^ "Bacterial Pathogenesis at Washington University". StudyBlue. סנט לואיס. הוחזר 2016-12-02.
- ^ "Print Friendly". www.lifeextension.com. הועבר לארכיון מ המקורי on 2016-12-02. הוחזר 2016-12-02.
- ^ Reddy M, Gill SS, Wu W, et al. (Feb 2012). "האם לחולה זה יש זיהום של פצע כרוני?". ג'אמה. 307 (6): 605–11. דוי:10.1001 / jama.2012.98. PMID 22318282.
- ^ http://www.immunize.org/catg.d/p4215.pdf
- ^ Chronic Infection Information Retrieved on 2010-01-14 הועבר בארכיון 22 ביולי 2015, ב מכונת Wayback
- ^ טפילי מעיים וזיהום הועבר בארכיון 28/10/2010 ב מכונת Wayback fungusfocus.com - אוחזר בתאריך 21/01/2010
- ^ "Clinical Infectious Disease – Introduction". www.microbiologybook.org. הוחזר 2017-04-19.
- ^ Pathogens and vectors. MetaPathogen.com.
- ^ Seventer JM, Hochberg NS (October 2016). "Principles of Infectious Diseases: Transmission, Diagnosis, Prevention, and Control". אנציקלופדיה בינלאומית לבריאות הציבור: 22–39. דוי:10.1016/B978-0-12-803678-5.00516-6. ISBN 9780128037089. PMC 7150340.
- ^ Ljubin-Sternak, Suncanica; Mestrovic, Tomislav (2014). "סקירה: Chlamydia trachonmatis ו- Mycoplasmias של איברי המין: פתוגנים עם השפעה על בריאות הרבייה האנושית". Journal of Pathogens. 2014 (183167): 3. דוי:10.1155/2014/183167. PMC 4295611. PMID 25614838.
- ^ א ב Van den Bruel A, Haj-Hassan T, Thompson M, Buntinx F, Mant D (March 2010). "Diagnostic value of clinical features at presentation to identify serious infection in children in developed countries: a systematic review". אִזְמֵל. 375 (9717): 834–45. דוי:10.1016/S0140-6736(09)62000-6. PMID 20132979. S2CID 28014329.
- ^ Bloomfield SF, Aiello AE, Cookson B, O'Boyle C, Larson EL (2007). "The effectiveness of hand hygiene procedures including hand-washing and alcohol-based hand sanitizers in reducing the risks of infections in home and community settings". כתב העת האמריקני לבקרת זיהומים. 35 (10): S27–S64. דוי:10.1016/j.ajic.2007.07.001. PMC 7115270.
- ^ ""Generalized Infectious Cycle" Diagram Illustration". science.education.nih.gov. הועבר לארכיון מ המקורי בתאריך 24/09/2009. הוחזר 2010-01-21.
- ^ א ב ווטס, דאנקן (2003). Six degrees: the science of a connected age. לונדון: ויליאם היינמן. ISBN 978-0-393-04142-2.
- ^ Preston, Richard (1995). The hot zone. Garden City, N.Y.: Anchor Books. ISBN 978-0-385-49522-6.
- ^ Ferguson NM, Donnelly CA, Anderson RM (May 2001). "The foot-and-mouth epidemic in Great Britain: pattern of spread and impact of interventions". מַדָע. 292 (5519): 1155–60. ביבקוד:2001Sci ... 292.1155F. דוי:10.1126 / science.1061020. PMID 11303090. S2CID 16914744.
- ^ Barreto ML, Teixeira MG, Carmo EH (2006). "Infectious diseases epidemiology". כתב העת לאפידמיולוגיה ובריאות הקהילה. 60 (3): 192–95. דוי:10.1136/jech.2003.011593. PMC 2465549. PMID 16476746.
- ^ Ge D, Fellay J, Thompson AJ, Simon JS, Shianna KV, Urban TJ, Heinzen EL, Qiu P, Bertelsen AH, Muir AJ, Sulkowski M, McHutchison JG, Goldstein DB (2009). "וריאציה גנטית ב- IL28B מנבאת אישור ויראלי המושרה על ידי הפטיטיס C". טֶבַע. 461 (7262): 399–401. ביבקוד:2009 Natur.461..399G. דוי:10.1038 / nature08309. PMID 19684573. S2CID 1707096.
- ^ Thomas DL, Thio CL, Martin MP, Qi Y, Ge D, O'Huigin C, Kidd J, Kidd K, Khakoo SI, Alexander G, Goedert JJ, Kirk GD, Donfield SM, Rosen HR, Tobler LH, Busch MP, McHutchison JG, Goldstein DB, Carrington M (2009). "וריאציה גנטית ב- IL28B ובפינוי ספונטני של נגיף הפטיטיס C". טֶבַע. 461 (7265): 798–801. ביבקוד:2009 טבע 461..798 ת. דוי:10.1038 / nature08463. PMC 3172006. PMID 19759533.
- ^ Fair RJ, Tor Y (2014). "Antibiotics and Bacterial Resistance in the 21st Century". Perspectives in Medicinal Chemistry. 6: 25–64. דוי:10.4137/PMC.S14459. PMC 4159373. PMID 25232278. הוחזר 13 במאי 2020.
- ^ "Antibiotics: List of Common Antibiotics & Types". Drugs.com. הוחזר 2020-11-10.
- ^ O'Brien, Deirdre J.; Gould, Ian M. (August 2013). "Maximizing the impact of antimicrobial stewardship". חוות הדעת הנוכחית במחלות זיהומיות. 26 (4): 352–58. דוי:10.1097/QCO.0b013e3283631046. PMID 23806898. S2CID 5487584.
- ^ ארגון הבריאות העולמי (פברואר 2009). "Age-standardized DALYs per 100,000 by cause, and Member State, 2004".
- ^ "Could Ebola rank among the deadliest communicable diseases?". חדשות CBC. 20 באוקטובר 2014.
- ^ "The World Health Report (Annex Table 2)" (PDF). 2004.
- ^ "Table 5" (PDF). 1995.
- ^ Lower respiratory infections include various pneumonias, השפעות ו ברונכיטיס חריפה.
- ^ Diarrheal diseases are caused by many different organisms, including כּוֹלֵרָה, בּוּטוּלִיזְם, ו אי - קולי עד כמה שם. See also: Intestinal infectious diseases
- ^ Tropical diseases include מחלת שאגאס, קדחת דנגי, פילאריאזיס לימפתי, לישמניאזיס, אונצ'וקרציאזיס, סכיסטוזומיאזיס ו trypanosomiasis.
- ^ "WHO | The top 10 causes of death". מי. הוחזר 2015-09-24.
- ^ Fauci AS, Morens DM (2012). "The perpetual challenge of infectious diseases". כתב העת לרפואה של ניו אינגלנד. 366 (5): 454–61. דוי:10.1056/NEJMra1108296. PMID 22296079.
- ^ "Infectious and Epidemic Disease in History" הועבר בארכיון 12 ביולי 2012, בשעה Archive.today
- ^ א ב Dobson AP, Carter ER (1996). "Infectious Diseases and Human Population History" (PDF). BioScience. 46 (2): 115–26. דוי:10.2307/1312814. JSTOR 1312814.
- ^ "אֲבַעבּוּעוֹת". North Carolina Digital History.
- ^ Smallpox and Vaccinia. National Center for Biotechnology Information. הועבר בארכיון 1 ביוני, 2009, ב מכונת Wayback
- ^ Barquet, Nicolau (15 October 1997). "Smallpox: The Triumph over the Most Terrible of the Ministers of Death". תולדות הרפואה הפנימית. 127 (8_Part_1): 635–42. דוי:10.7326/0003-4819-127-8_Part_1-199710150-00010. PMID 9341063. S2CID 20357515.
- ^ Multidrug-Resistant "Tuberculosis". מרכזים לבקרת מחלות ומניעתן. הועבר בארכיון March 9, 2010, at the מכונת Wayback
- ^ "Influenza of 1918 (Spanish Flu) and the US Navy". 20 February 2006. Archived from המקורי ב -20 בפברואר 2006.
- ^ א ב Krauss H; Weber A; Appel M (2003). Zoonoses: Infectious Diseases Transmissible from Animals to Humans (מהדורה שלישית). וושינגטון הבירה: ASM Press. ISBN 978-1-55581-236-2.
- ^ Potter P (July 2013). "Summer buzz". Disg Infect Dis. 19 (3): 1184. דוי:10.3201/eid1907.AC1907. PMC 3903457.
- ^ Peter Daszak; Andrew A. Cunningham; Alex D. Hyatt (27 January 2000). "Emerging Infectious Diseases of Wildlife – Threats to Biodiversity and Human Health". מַדָע. 287 (5452): 443–49. ביבקוד:2000Sci...287..443D. דוי:10.1126/science.287.5452.443. PMID 10642539.
- ^ Singer, Charles and Dorothea (1917) "The scientific position of Girolamo Fracastoro [1478?–1553] with especial reference to the source, character and influence of his theory of infection," תולדות ההיסטוריה הרפואית, 1 : 1–34; ראה עמ ' 14.
- ^ Thucydides with Richard Crawley, trans., היסטוריה של מלחמת פלופונסיה (London: J.M. Dent & Sons, Ltd., 1910), Book III, § 51, עמ '131–32.
- ^ Nutton, Vivian (1983) "The seeds of disease: an explanation of contagion and infection from the Greeks to the Renaissance," היסטוריה רפואית, 27 (1) : 1–34; ראה עמ ' 10. Available at: הספרייה הלאומית לרפואה בארה"ב, המכונים הלאומיים לבריאות
- ^ Rastogi, Nalin; Rastogi, R (1985-01-01). "Leprosy in ancient India". International Journal of Leprosy and Other Mycobacterial Diseases. 52 (4): 541–43. PMID 6399073.
- ^ Susruta; Bhishagratna, Kunja Lal (1907–1916). An English translation of the Sushruta samhita, based on original Sanskrit text. Edited and published by Kaviraj Kunja Lal Bhishagratna. With a full and comprehensive introd., translation of different readings, notes, comparative views, index, glossary and plates. Gerstein – University of Toronto. כלכותה.
- ^ Hoernle, A. F. Rudolf (August Friedrich Rudolf) (1907). Studies in the medicine of ancient India. Gerstein – University of Toronto. Oxford : At the Clarendon Press.
- ^ בירן, ג'וזף פטריק (2012). אנציקלופדיה של המוות השחור. ABC-CLIO. עמ ' 29. ISBN 978-1598842531.
- ^ Reid, Megan H. (2013). Law and Piety in Medieval Islam. הוצאת אוניברסיטת קיימברידג '. pp. 106, 114, 189–90. ISBN 978-1107067110.
- ^ Majeed, Azeem (22 December 2005). "איך האיסלאם שינה את הרפואה". BMJ. 331 (7531): 1486–87. דוי:10.1136 / bmj.331.7531.1486. ISSN 0959-8138. PMC 1322233. PMID 16373721.
- ^ ברטה M (2003). "תחיית האטומיזם הלוקרטיאני והמחלות המדבקות בתקופת הרנסנס". Medicina Nei Secoli. 15 (2): 129–54. PMID 15309812.
- ^ מורהד רוברט (נובמבר 2002). "ויליאם באד וטיפוס הבטן". J R Soc Med. 95 (11): 561–64. דוי:10.1258 / jrsm.95.11.561. PMC 1279260. PMID 12411628.
- ^ סרפד D (2009). "השפעות אקולוגיות על המגוון ההתנהגותי האנושי: סקירת הממצאים האחרונים". מגמות אקול. Evol. 24 (11): 618–24. דוי:10.1016 / j.tree.2009.05.013. PMID 19683831.
- ^ Molnar, R. E., 2001, "Theropod paleopathology: סקר ספרות": ב: חיי חוליות מזוזואיים, בעריכת טאנקה, ד.ה., ונגר, ק ', הוצאת אוניברסיטת אינדיאנה, עמ' 337–63.
- ^ קספרמאייר, ג'ו (23 בספטמבר 2007). "הוכח כי מעוף חלל משנה את יכולתם של חיידקים לגרום למחלות". אוניברסיטת אריזונה. הוחזר 14 בספטמבר 2017.
- ^ קים וו, ואח '. (29 באפריל 2013). "טיסה בחלל מקדמת היווצרות ביופילם מאת פסאודומונס אירוגינוזה". PLOS ONE. 8 (4): e6237. ביבקוד:2013PLoSO ... 862437K. דוי:10.1371 / journal.pone.0062437. PMC 3639165. PMID 23658630.
- ^ דבורסקי, ג'ורג '(13 בספטמבר 2017). "מחקר מדאיג מציין מדוע חיידקים מסוימים עמידים יותר לתרופות בחלל". גיזמודו. הוחזר 14 בספטמבר 2017.
- ^ מינון, ק '; ביוגר-מינון, א '; דילמן, ר '; גיל, מ '; קרס, או. קליין, א .; מיינרט, ה '; נוארות, ט .; ריסי, ש. Stridde, C. (1995). ביוכימיה בחלל "ERA-experiment""" (PDF). התקדמות בחקר החלל. 16 (8): 119–29. ביבקוד:1995AdSpR..16..119D. דוי:10.1016 / 0273-1177 (95) 00280-R. PMID 11542696.[קישור מת קבוע ]
- ^ הורנק ז '; אשווילר, ארצות הברית; רייץ, ג '; וונר, י. וילימק, ר '; שטראוך, ק '(1995). "תגובות ביולוגיות לחלל: תוצאות הניסוי" היחידה האקסוביולוגית "של ה- ERA ב- EURECA I". עו"ד שטח מילואים. 16 (8): 105–18. ביבקוד:1995AdSpR..16..105H. דוי:10.1016 / 0273-1177 (95) 00279-נ. PMID 11542695.
קישורים חיצוניים
| מִיוּן |
|---|
- המרכז האירופי למניעת ובקרת מחלות
- מרכזים בארה"ב לבקרת מחלות ומניעתן,
- האגודה למחלות זיהומיות באמריקה (IDSA)
- מדד מחלות זיהומיות הסוכנות לבריאות הציבור בקנדה (PHAC)
- מרכז מחקר חיסונים מידע הנוגע לניסויים קליניים במחקר חיסונים במחלות זיהומיות מתעוררות ומתעוררות מחדש.
- הַדבָּקָה משאב מידע
- חיידקים וזיהום (כתב עת)
- מקור ידע לאנשי מקצוע בתחום הבריאות העוסקים בניהול פצעים www.woundsite.info
- טבלה: מקרי מוות גלובליים ממחלות מדבקות, 2010 - חברת השידור הקנדית



